引言
想象一下某天,你终于拥有了心仪的房子,搬家公司的卡车已经满载着家具抵达楼下,却发现搬家师傅不停对你摇头。那台刚买不久的双开门冰箱,那个奶奶留下的雕花红木衣柜,那个你斥巨资全款到手的巨型手办,通通卡在单元门框前,纹丝不动。“东西是好东西,但门太小,进不去。”这就是基因治疗领域长期面临的尴尬处境。
腺相关病毒(AAV)因其安全性高、免疫原性低、能长期表达等优势,被誉为基因治疗的“金牌搬家公司”。截至目前,已有超过8款AAV基因药物获批上市。然而,AAV有一个致命的短板:包装容量仅约4.7 kb。但超过37.5%与自闭症谱系障碍(ASD)密切相关的致病基因,其编码序列都超过了4 kb。基因治疗的大门,对这些患者似乎关上了一半。
2026年1月27日,中国科学院深圳先进技术研究院路中华团队在Cell上发表了题为“AAVLINK: A potent DNA-recombination method for large cargo delivery in gene therapy”的研究。该研究开发了一种基于Cre/loxP位点特异性DNA重组的AAV递送策略——AAVLINK,该系统能够高效、精确地将大基因分割包装进多个AAV载体,并在靶细胞内通过DNA重组与RNA剪接恢复全长基因功能,为大基因治疗提供了强大的通用型平台。
一、AAVLINK的设计原理与优化验证
一切创新始于精巧的设计。AAVLINK系统的核心在于将目的基因(GOI)拆分为5'端和3'端两部分,分别包装于两个AAV载体。当两载体共转导同一细胞后,Cre首先表达并催化lox位点间的分子间重组,将GOI 5'端-SD模块与剪接受体(SA)-GOI 3'端模块连接。重组完成后,Cre编码序列被从poly(A)信号上游“切除”,其表达随之衰减;同时,通过RNA剪接去除内含子序列,生成全长GOI mRNA。这一设计实现了重组驱动的Cre自沉默和剪接依赖的精准读码框恢复,为后续所有实验奠定了方法论基础。
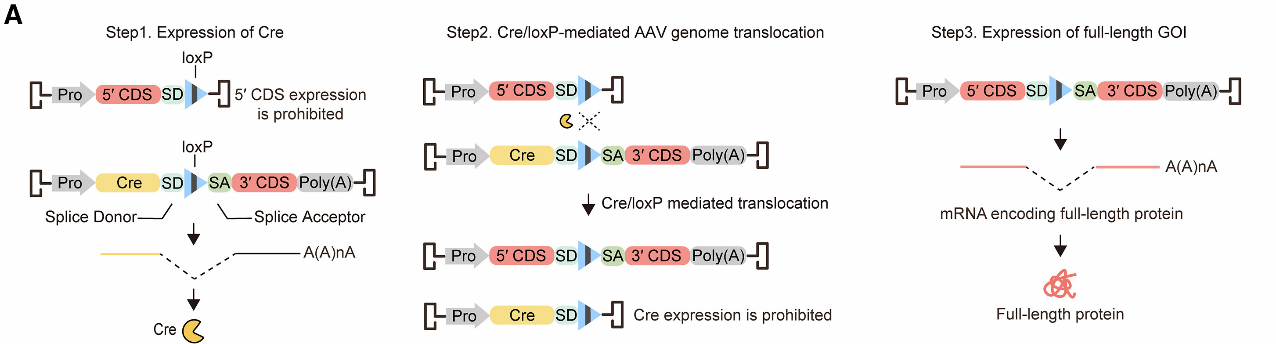
图1 AAVLINK的设计原理
二、三重载体系统的构建与验证
对于超过双载体容量极限的更大基因,AAVLINK可扩展为三重载体系统。该设计使用两对正交lox位点——第一对介导5'端与中间体片段的连接,第二对携带lox2272间隔区突变的lox位点介导中间体与3'端的连接,从而避免不同lox对之间的交叉反应(图2A-B)。研究者将TagRFP基因拆分为三段并分别装入三个AAV载体,小鼠和食蟹猴大脑皮层的体内实验证实了其可行性。三重AAVLINK系统的理论最大递送容量可达约11 kb,覆盖绝大多数人类疾病相关基因的编码序列。
此外研究者还发现,无论体外还是体内,AAVLINK的重组效率均对现有intein方法及StitchR技术形成数量级优势。同时在疾病相关基因的递送测试中,AAVLINK同样展现出压倒性优势。
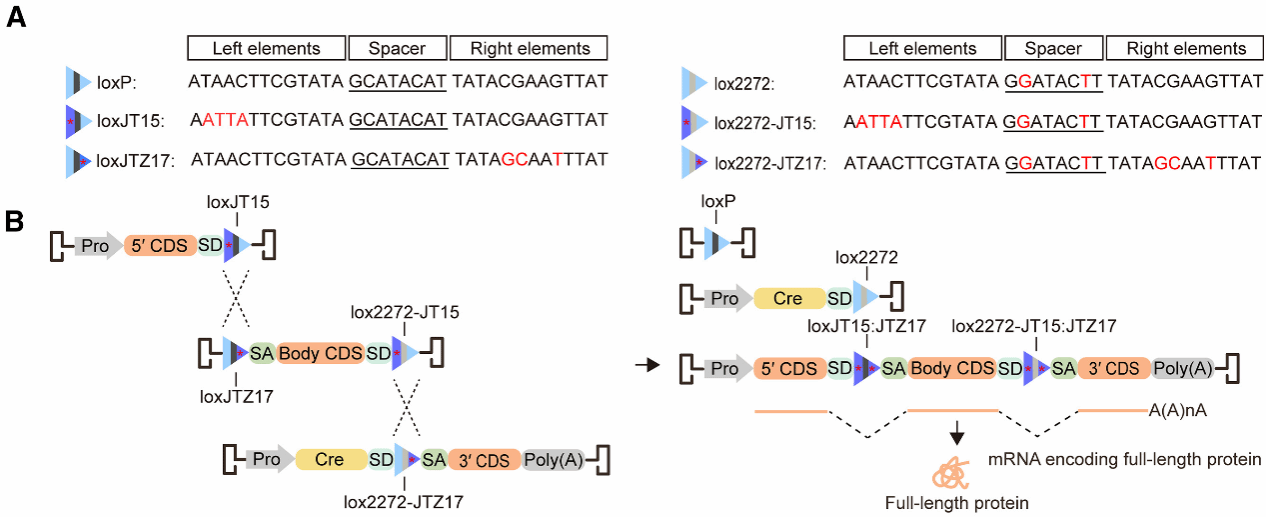
图2 AAVLINK实现三载体基因载荷的成功递送
三、AAVLINK的疾病治疗验证
性能优势既已确立,那么这种技术能否在真实的疾病模型中产生治疗效果?研究团队选择了两类由超大基因突变导致的代表性单基因疾病进行疗效验证。在Phelan-McDermid综合征(PMS)的应用中,接受Shank3替代治疗的小鼠重复刻板行为(自我梳理时间)显著减少,转棒实验的运动协调能力也明显改善(图3F)。这一结果首次证明,AAVLINK介导的局部脑区基因替代足以挽救PMS的核心行为表型。
Dravet综合征主要由SCN1A半量不足引起。SCN1A基因全长6 kb,超过AAV载荷上限,但其单基因致病特性适合基因替代治疗。研究者首先构建了Scn1a功能缺失小鼠模型,该模型表现出温度依赖性癫痫发作和中位生存期仅21天的严重表型。治疗后,小鼠生存率显著提高,热诱导癫痫阈值温度升高(图3K)。
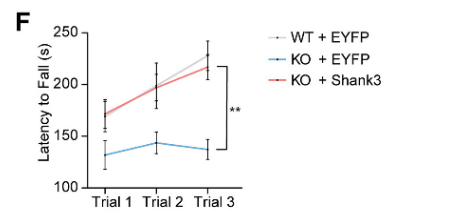
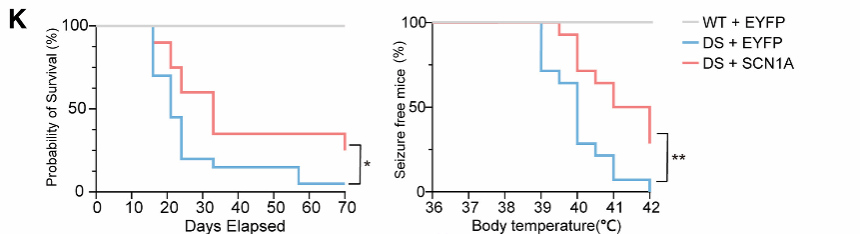
图3 AAVLINK介导的基因替代治疗在PMS和Dravet综合征小鼠模型中的应用
四、AAVLINK递送多种CRISPR-Cas工具的能力验证
CRISPR-Cas系统在基因治疗中潜力巨大,但其大尺寸同样面临AAV包装瓶颈。研究者将SpCas9在c.2682位点拆分并装入双AAVLINK载体,在体外COS-7细胞及体内小鼠肝脏中均成功实现了基因编辑。
对于更精细的碱基编辑器,ABE8e(A→G编辑)在c.2964位点拆分后,AAVLINK递送在HEK293T细胞中实现了高达80%的编辑效率;小鼠肝脏中Pcsk9基因的编辑率达16%,并伴随Pcsk9蛋白水平显著下降(图4K)。YE1-BE4max(C→T编辑)在c.3540位点拆分后同样成功实现多靶点高效编辑。此外,AAVLINK还成功递送了CRISPRoff-V2(转录抑制)和dSpCas9-VPH(转录激活)系统,前者显著下调RHOXF2、ASCL1等基因表达,后者在小鼠海马中成功激活Scn1a转录(图4L)。这些结果全面展示了AAVLINK作为通用型大尺寸基因编辑工具递送平台的潜力。
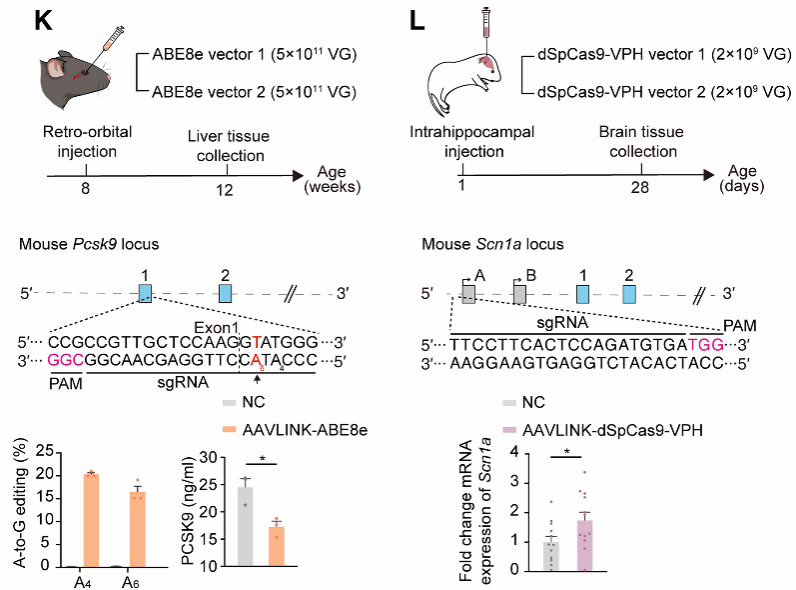
图4 AAVLINK介导的CRISPR工具递送
五、AAVLINK2.0消除Cre毒性隐忧
尽管AAVLINK中Cre表达具有自限性,但未重组细胞中残留的Cre活性仍可能引发DNA损伤和细胞毒性。为此,研究者通过两步策略开发了AAVLINK2.0(图5)。第一步筛选出SCP1(Super Core Promoter 1)启动子,将Cre蛋白水平降至最低。第二步在Cre的C末端融合UDeq3a蛋白降解决定子标签,大幅缩短其半衰期。
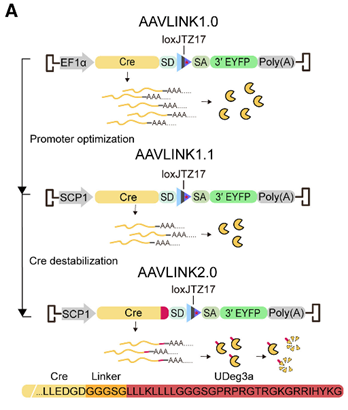
图5 AAVLINK2.0中Cre表达的最小化
小鼠颅内立体定位注射和全身静脉注射后,AAVLINK2.0的Cre表达不可检出,而目的基因EYFP的表达依然稳定(图6L)。在食蟹猴大脑皮层中,AAVLINK2.0同样实现了“Cre表达不可检测、目的基因高效重组”的理想状态(图6N)。这一安全升级显著降低了Cre相关毒性风险,为AAVLINK的临床转化扫清了重要障碍。
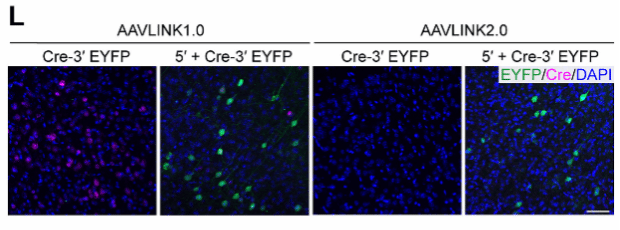
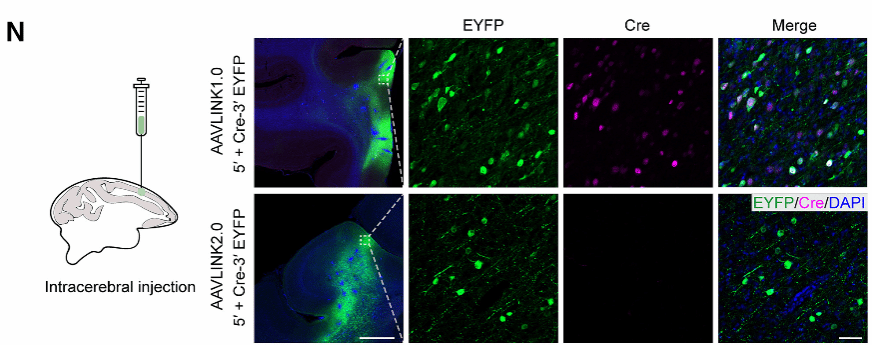
图6 AAVLINK2.0在体内表达情况
六、198个疾病相关大基因的AAVLINK载体资源库
为充分发挥AAVLINK的应用价值,研究者构建了一个涵盖193个疾病相关大基因和5个CRISPR工具载体的资源库。基因选取标准聚焦于编码序列长度在3.9 kb至11.1 kb之间的单基因病致病基因,重点关注自闭症谱系障碍(ASD)风险基因(166个)及其他代表性单基因病基因(27个,如AGL、OTOF、DMD等)。所有基因均被克隆至AAVLINK1.0载体并同步改造为AAVLINK2.0版本。
所有载体信息已整理至公开网站http://AAVLINK.com,供全球研究者免费查阅和申请。这一资源库的建立,将AAVLINK从“一项实验室技术”升维为“一个开放共享的基因治疗基础设施”。
总结与展望
AAVLINK技术的诞生,为基因治疗领域带来了三重突破:相较现有intein和StitchR方法,重组效率提升数倍至数百倍;几乎不产生截短蛋白副产物,避免显性负效应;AAVLINK2.0将Cre表达降至不可检测水平,消除致癌风险隐忧。在Phelan-McDermid综合征和Dravet综合征两种难治性神经系统疾病的小鼠模型中,AAVLINK均展现出显著的治疗效果。
根据世界卫生组织数据,全球约有3亿罕见病患者,其中约80%由基因缺陷引起。对于许多超大基因突变导致的疾病(如Duchenne肌营养不良、囊性纤维化、Usher综合征等),AAV的容量限制一直是基因替代疗法难以逾越的鸿沟。AAVLINK的成功,意味着这些“大基因病”终于有了一种高效、安全的递送方案。特别是研究团队公开的198个基因载体资源库,将极大加速相关疾病基因治疗的研究进程。
我们有理由相信,在不远的将来,那些曾经因为“基因太大装不下”而被基因治疗拒之门外的疾病,将迎来属于它们的黎明。
参考文献
[1] Mich JK, Ryu J, Wei AD, et al. Interneuron-specific dual-AAV SCN1A gene replacement corrects epileptic phenotypes in mouse models of Dravet syndrome. Sci Transl Med. 2025;17(790):eadn5603.
[2] Lindley SR, Subbaiah KCV, Priyanka F, et al. Ribozyme-activated mRNA trans-ligation enables large gene delivery to treat muscular dystrophies. Science. 2024;386(6723):762-767.
[3] Tornabene P, Trapani I, Minopoli R, et al. Intein-mediated protein trans-splicing expands adeno-associated virus transfer capacity in the retina. Sci Transl Med. 2019;11(492):eaav4523.
原文链接:https://doi.org/10.1016/j.cell.2025.12.039IF: 42.5 Q1
AAVLINK载体资源库:http://AAVLINK.com
作者:谢志勇组 李赫群