一、引言
你是否有过这样的感受:每天都丧丧的,对什么事情都提不起兴趣,每天的生活只会让你感到日复一日的无趣,曾经所热爱的事情也变得黯然失色,不想出门社交只想躺平,无欲无求,生活呈现一种淡淡的死意。如果你正在经历这样的状态,你可能要警惕,你正面临”快感缺失”的心理挑战。

 (插图)
(插图)
快感缺失(Anhedonia),是重度抑郁症、成瘾和精神分裂症的核心症状。美国精神病学会制定的《精神障碍诊断与统计手册》第5版(DSM-5)对快感缺失的定义是:对全部或几乎全部的活动失去兴趣、对平常的快乐刺激失去反应。如果一个人长期(至少持续两周)经历快感缺失,就可能会被诊断为抑郁症。
快乐的人总是相似的,而快感缺失的人各有各的不幸——李夫·托尔斯靖。
快感缺失有3种的常见类型:
①完成型快感缺失:目标达成后却感受不到满足和成就感,如机械般工作的社畜;
②动机型快感缺失:对有趣事物失去兴趣,处于低多巴胺状态,如电子ED人群。
③社交型快感缺失:与人互动不仅不快乐,反而感到焦虑,习惯独处,拒绝社交。
快感源自大脑的奖赏中心,包括腹侧被盖区、伏隔核、前额叶、海马和杏仁核,这些特定的大脑结构及其形成的神经网络。它通过产生正向的体验和愉悦感,帮助我们建立与奖赏相关的记忆和联想,并影响我们的决策,促使我们向奖赏性的刺激靠近1。做对生存有利的事情如吃美食时,大脑的奖赏系统会分泌多巴胺释放到不同脑区,让我们感到快乐和满足,并且让我们下次还想吃。
那么,快感缺失是如何产生的呢?目前研究表明,在抑郁症患者中,奖赏神经环路中的前扣带皮层(anterior cingulate cortex ,ACC)的功能障碍与快感缺失高度相关2。ACC会向伏隔核(nucleus accumbens,NAc)形成密集的投射,并与各种奖赏信息的处理功能有关。然而,我们对于大脑通过编码努力信号和调节个体花费努力以获得奖励的意愿来塑造享乐处理的神经回路的理解还不够完善。
2023年12月,美国威尔康奈尔医学院的 Conor Liston团队在Neuron上发表的研究,让我们对动机型快感缺失的神经环路机制有了进一步的清晰认识,题为A stress-sensitive frontostriatal circuit supporting effortful reward-seeking behavior。这篇研究揭示了在寻求奖励的行为中,ACC-NAc关键环路如何支持努力评估(effort valuation)以及未来努力分配,以获得最大化奖励的决策,阐明了慢性应激导致的动机型快感缺失的环路机制3。

二、结果
1、ACC对于整合不同奖励和努力价值的决策是必要的
在这项研究中,研究者设计了一个基于努力的的T迷宫决策范式,在两个目标臂放置不同体积的饮用水,高奖励的一端将引入一个可攀爬的障碍物来增加获取难度,通过不同体积的饮用水和可攀爬的障碍物来评估小鼠对努力和奖励的权衡与决策(图1A-B)。研究发现,ACC脑区在这一过程中扮演着关键角色。抑制ACC活动后,小鼠不再被高奖励吸引,转而迟缓地寻求低奖励。(图1 F-K)。
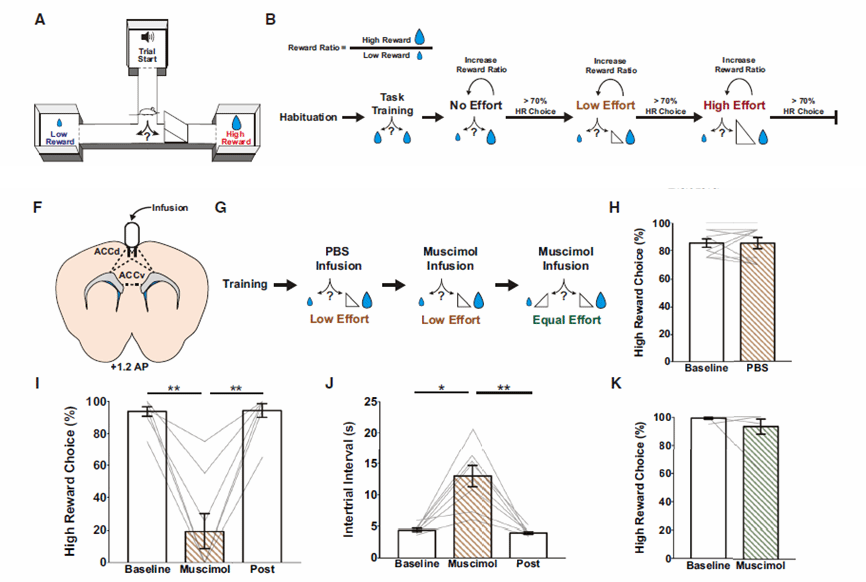
图1 ACC对于需要整合不同奖励和努力值的决策是必要的
2、ACC-NAc活动编码奖励相关信号
尽管ACC与众多脑区有着广泛连接,且ACC神经元是功能异质的,但汇集前人的研究提示了他们,向NAc投射的ACC神经元可能编码了努力相关信息来影响决策过程4。研究人员进一步发现,ACC往NAc投射的额叶纹状体环路编码了奖赏相关信号。钙成像结果显示,向NAc投射的ACC的神经元活动在决策、靠近和获得奖励的几个阶段发生显著变化(图2D)。在T迷宫任务中,ACC-NAc神经元活动在小鼠攀爬障碍物时开始上升,并在消耗努力的终点达到顶峰。这表明ACC-NAc活动同时编码了奖赏和努力相关的信息。
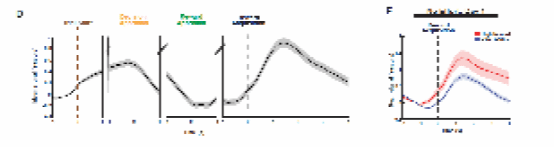
图2 ACC-NAc活动编码奖励相关信号
3、ACC-NAc的奖赏相关信号受先前努力的调节,并支持努力的奖赏寻求
基于此,研究人员继续提出问题: 在T迷宫任务中ACC-NAc活动是否也编码与努力相关的信息?这些努力相关信息是否被整合进奖励相关的活动中?还是在决策点之前单独出现?
对低努力和高努力阶段的钙成像结果表明,ACC-NAc神经元活动在小鼠攀爬障碍物时开始上升,在消耗努力的终点——爬上障碍物的顶端时达到顶峰。并且,小鼠在经历磨难得到更高奖励的试验中,ACC-NAc神经元活动水平显著高于低奖励试验(图3 D-E)。因此,ACC-NAc活动同时编码了奖赏和努力相关的信息。
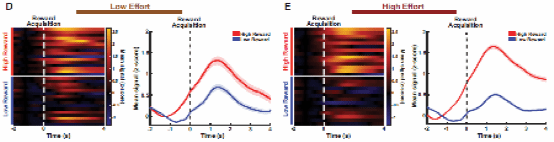
图3 ACC-NAc的奖励相关信号受到先前努力的调节
4、ACC-NAc活动支持未来需要努力的决策
研究者通过光遗传学工具在不同阶段抑制ACC-NAc神经元活动,发现只有在努力后-得到高奖励前的这一阶段,这条环路的活动会显著下降,并且光抑制后降低了小鼠在后续试验中做出高努力选择的次数(图4 C-G)。这些结果表明,ACC-NAc信号起始于努力消耗之后,获得奖励之前,其在奖励期的持续可能对支持未来的努力决策起着重要作用。
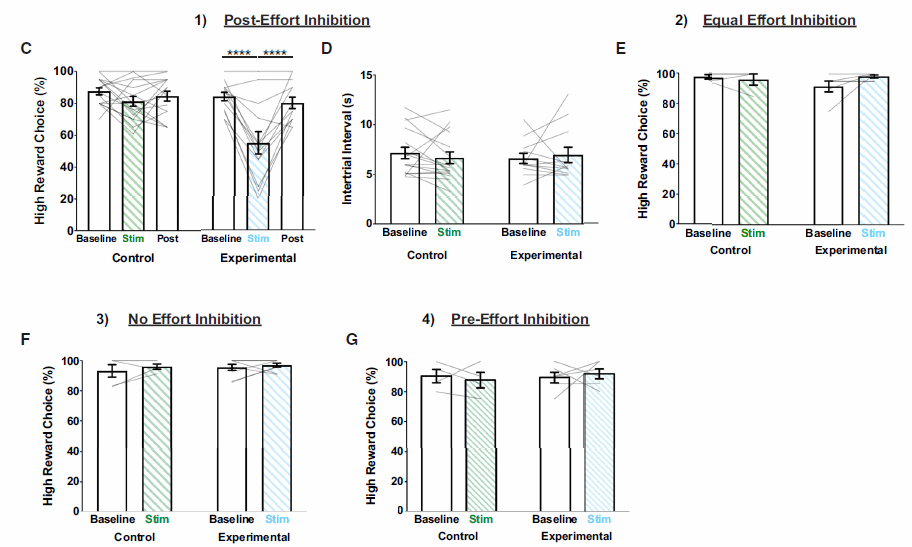
图4 ACC-NAc活动支持未来努力决策
5、慢性应激破坏了消耗努力的奖励寻求反应和ACC-NAc功能
先前的研究表明,慢性应激会抑制啮齿类动物的寻求奖励行为4。ACC神经元在慢性应激状态下会发生树突收缩和突触丧失。为进一步研究ACC-NAc环路功能与慢性应激的关系,经过慢性皮质酮暴露的小鼠大大降低了消耗努力去追求高奖励的意愿(图5 B-C)。并且,在无需努力的条件下,应激小鼠对高奖励的追求不受影响(图5D)。这些结果重复了蝇蕈醇实验引发的破坏效应(图1),提示慢性皮质酮暴露干扰了对追求最大化奖励时的最佳努力分配。
他们还发现,经过慢性皮质酮暴露后,ACC-NAc对经过努力后获得奖励的钙信号反应变得钝化,甚至无法区分低奖励和高奖励(图5E-G)。这些结果表明,慢性应激状态引发的动机性快感缺失与由ACC-NAc功能障碍高度相关。
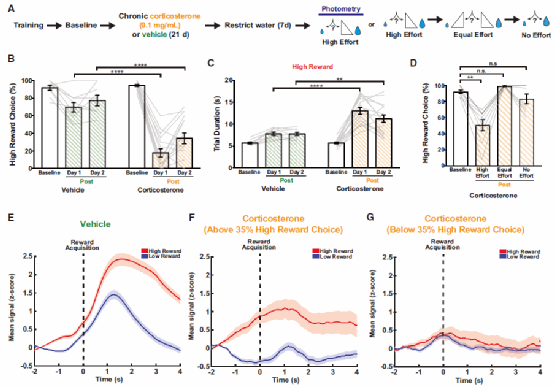
图5 慢性应激改变努力决策和损伤ACC-NAc环路功能
三、总结
这篇研究加深了人们对前扣带皮层-伏隔核(ACC-NAc)环路表征努力-激励相关信号和决策功能的认识。研究证实,在长期慢性应激的影响下,小鼠的神经内分泌反应发生变化,这不仅降低了它们的动机水平,抑制了消耗努力寻求奖励的行为,还破坏了ACC-NAc环路功能。目前临床对于快感缺失不存在针对性的药物治疗,因此,深入理解快感缺失的神经生物学机制对于确定精神分裂症和抑郁症的潜在治疗靶点具有重要意义。
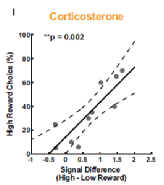
图6
原文链接:https://doi.org/10.1016/j.neuron.2023.10.020
参考文献
Uncategorized References
1 Berridge, K. C. & Kringelbach, M. L. Pleasure systems in the brain. Neuron 86, 646-664 (2015). https://doi.org/10.1016/j.neuron.2015.02.018
2 Pizzagalli, D. A. Depression, stress, and anhedonia: toward a synthesis and integrated model. Annu Rev Clin Psychol 10, 393-423 (2014). https://doi.org/10.1146/annurev-clinpsy-050212-185606
3 Fetcho, R. N. et al. A stress-sensitive frontostriatal circuit supporting effortful reward-seeking behavior. Neuron 112, 473-487 e474 (2024). https://doi.org/10.1016/j.neuron.2023.10.020
4 Hollon, N. G., Burgeno, L. M. & Phillips, P. E. M. Stress effects on the neural substrates of motivated behavior. Nature Neuroscience 18, 1405-1412 (2015). https://doi.org/10.1038/nn.4114
本文作者:谢志勇组李靖