引言
我们每天都会经历无数事情:一段对话、一幅画面、一次惊险的瞬间。但只有极少数,会在数周、数月甚至数年之后依然清晰存在,成为塑造“自我”的一部分。那么,一个短暂的经历,是如何在大脑中“扎根”,并抵抗时间侵蚀的?长期研究发现,记忆的形成并非一次完成,而是一个分阶段推进的过程[1]。在学习过程中,神经元突触处的钙离子内流和激酶激活可迅速增强突触功能,形成短期记忆;而要使记忆长期稳定,则必须启动新的基因转录和蛋白质合成。这些新合成的蛋白质能够重塑突触结构,例如促进树突棘生长和突触连接增强,从而将短暂的神经活动转化为持久的神经连接[2]。然而,仅有突触层面的变化仍不足以解释记忆为何能够持续数周甚至终生。大脑每天接收的信息远超其能够长期储存的容量,这意味着,记忆不仅需要被“增强”,还必须被“选择”。越来越多证据表明,记忆会随着时间推移逐渐从海马转移至皮层,实现长期储存[3]。但一个关键问题仍未解决:大脑是如何在分子和环路层面,选择哪些记忆能够被长期保留?
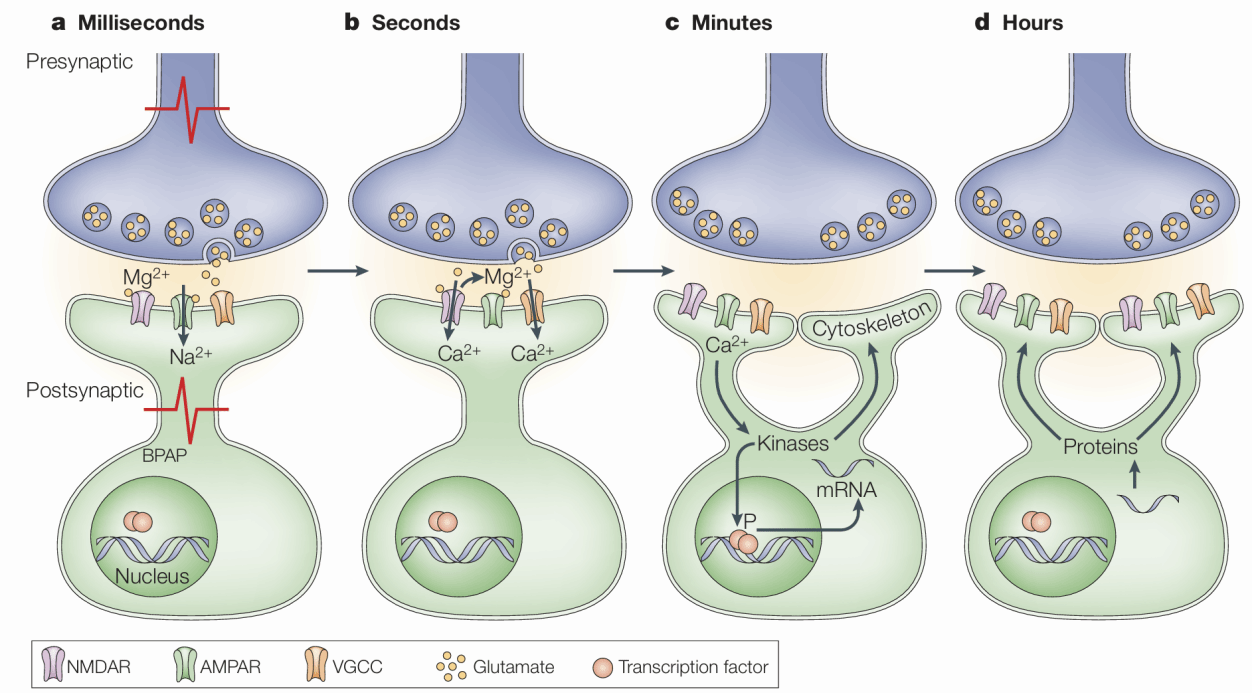
图 参与突触可塑性启动和维持的分子机制[2]
2025年11月26日,来自Rockefeller University的Priya Rajasethupathy研究团队在《Nature》期刊上发表了题为“Thalamocortical transcriptional gates coordinate memory stabilization”的研究,首次揭示丘脑与皮层之间存在一种跨脑区的“转录门控机制”,能够协调基因表达程序,从而选择性地稳定长期记忆。这一发现表明,记忆的持久性不仅取决于突触是否被成功激活,更取决于跨脑区转录调控网络是否“允许”该记忆进入长期储存状态,即记忆的持久性不仅取决于“写入”是否成功,更取决于大脑是否“允许它留下”。这一研究为理解记忆如何从短暂体验转化为持久印象,提供了全新的分子与环路机制视角。

1. HPC–ANT–ACC环路调控记忆巩固
为了研究大脑如何选择长期记忆,研究者建立了一种基于虚拟现实(VR)的行为范式,使小鼠能够形成多种情境记忆,但只有部分记忆最终被长期保留。在实验中,小鼠经历两种与水奖励相关的情境:一种重复次数较多(high repetition, HR),更容易形成“深刻记忆”;另一种重复次数较少(low repetition, LR),对应“短暂记忆”。此外,还设置了一种与空气喷吹相关的厌恶情境(图1a)。行为结果显示,在近期(第1天),小鼠能够回忆起这两种奖励记忆;但在远期(第21天),只有“深刻记忆”仍然稳定存在,而“短暂记忆”则逐渐消失(图1b)。这说明,大脑并不会平等地保存所有记忆,而是会对记忆进行选择性保留。考虑到记忆巩固依赖于海马向皮层的转移,研究者利用光遗传学操纵神经环路。结果发现,在训练期间抑制海马(HPC)或内嗅皮层(EC)→前扣带皮层(ACC)投射,会影响记忆形成;抑制前丘脑(ANT)→前扣带皮层投射,则显著损害远期记忆,而激活该投射,甚至可以恢复原本趋于遗忘的“短暂记忆”(图1e, g–h)。
这些结果表明,海马主要参与记忆的初始形成,而丘脑与皮层之间的环路则在后期发挥关键作用,决定哪些记忆能够被长期稳定保存。
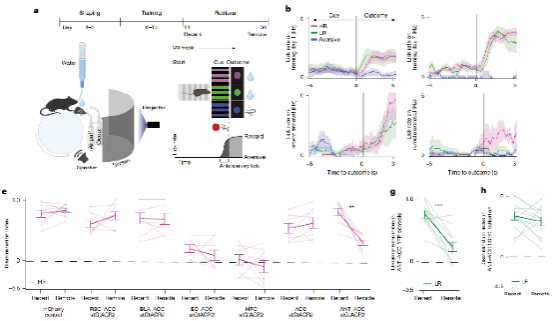
图1 监测记忆持久性的行为任务依赖于HPC、ANT和ACC
2. ANT和ACC在记忆稳定过程中激活不同的转录程序
既然丘脑-皮层环路决定记忆是否能够长期保存,那么其背后的分子基础是什么?为此,研究者在记忆形成后的不同时间点,对ANT–ACC环路神经元进行单细胞RNA测序分析(图2a)。结果显示,代表“深刻记忆”和“短暂记忆”的神经元,在近期记忆阶段就已出现不同的基因表达模式,甚至早于行为上记忆强度的差异,这说明 “深刻记忆”和“短暂记忆”神经元可能在早期就已经“走上不同轨道”(图2g–j)。进一步的通路分析发现,ANT中“深刻记忆”相关基因主要参与突触可塑性调控,并在记忆巩固中期达到峰值后逐渐下降,而ACC中“深刻记忆”相关基因则主要参与组蛋白甲基化相关通路,并持续活跃至远期阶段(图2l–o)。
以上结果揭示了一种跨脑区的分子“接力”模式:丘脑首先通过增强突触可塑性推动记忆进入巩固轨道,随后皮层通过染色质重塑,将这一短期可塑性状态转化为长期稳定的基因表达程序。
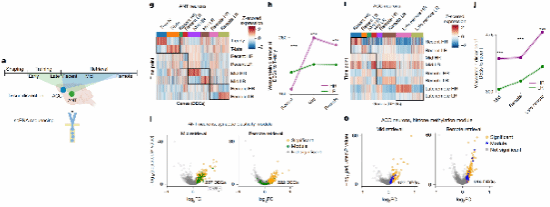
图2 与记忆维持相关的丘脑与皮层特异性程序
3. 转录调控因子驱动神经元进入与记忆持久性相关的稳定状态
为了进一步理解记忆稳定的分子基础,研究者利用拟时序分析,根据单细胞转录特征的连续性,推断神经元在记忆巩固过程中可能经历的状态转变轨迹。结果显示,在ANT中,“深刻记忆”神经元沿轨迹逐步进入新的转录状态;在ACC中,“深刻记忆”神经元在拟时序上的位置距离更远,提示其转录状态推进更为充分。相比之下,两脑区中“短暂记忆”神经元多停留在早期阶段(图3a–b, h–i)。这一现象提示,记忆能否长期保存,与神经元是否成功进入特定的稳定转录状态密切相关。进一步分析显示,这种状态转变由一系列关键转录调控因子驱动。在ANT中,CAMTA1、MYT1L、MEF2C和TCF4等转录因子参与不同阶段的巩固过程;而在ACC中,ASH1L、KMT2A和PRDM2等组蛋白甲基化相关因子则主要调控晚期巩固(图3d, k)。ATAC-seq结果进一步显示,这些转录因子相关调控模块的染色质可及性在巩固过程中显著增强,并以不同的激活程度持续存在(图3g, n)。
以上表明,长期记忆的形成不仅依赖神经元活动本身,还依赖转录调控网络推动神经元进入稳定的转录状态。
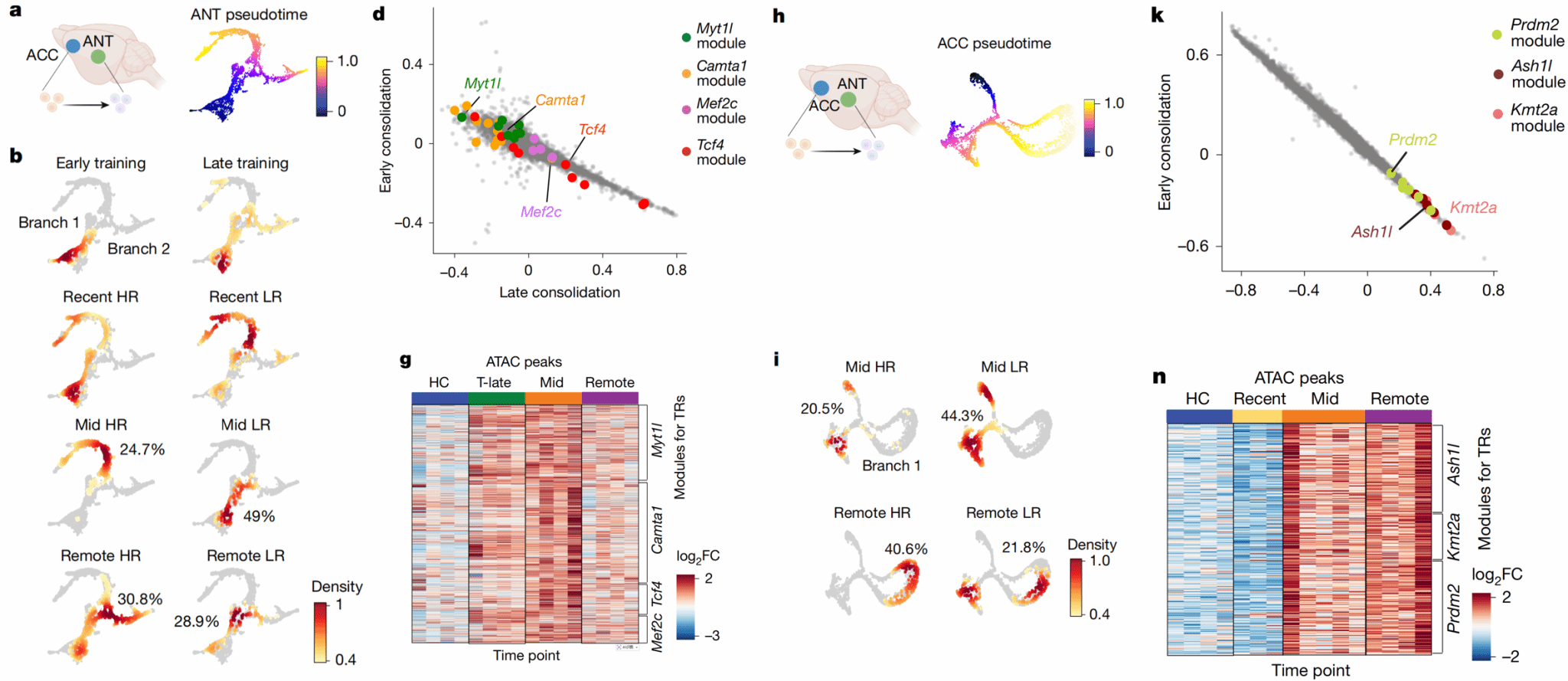
图3 转录调控因子驱动神经元进入与记忆持久性相关的状态
4. Camta1-Tcf4-Ash1l丘脑–皮层转录级联驱动记忆长期稳定
为了鉴定这些转录调控因子的功能,研究者利用CRISPR技术在特定脑区敲除相关基因。结果发现,在ANT中敲除Camta1会影响记忆巩固的中期阶段,而敲除Tcf4则显著损害远期记忆;在ACC中敲除Ash1l,则会选择性破坏远期记忆(图4e)。这表明,不同转录因子在不同阶段发挥时间窗口特异性的作用。钙信号记录进一步发现,敲除Camta1或Tcf4后,神经元活动变得更加随机,并降低ANT与ACC的功能相关性,提示这些转录因子在维持记忆相关神经环路稳定性中发挥重要作用(图4h)。结合ChIP–seq与拟时序分析显示,CAMTA1主要调控突触可塑性相关基因,参与记忆巩固的早期阶段;TCF4则调控细胞黏附与结构相关基因,使记忆表征在远期进一步稳定;而在ACC中,ASH1L通过H3K4me3重塑基因表达网络,使神经元由高度可塑状态过渡到结构稳定状态,并长期维持(图4i–j)。
综上,Camta1-Tcf4-Ash1l构成丘脑–皮层转录级联,通过阶段性调控不同基因模块,驱动记忆的长期稳定。
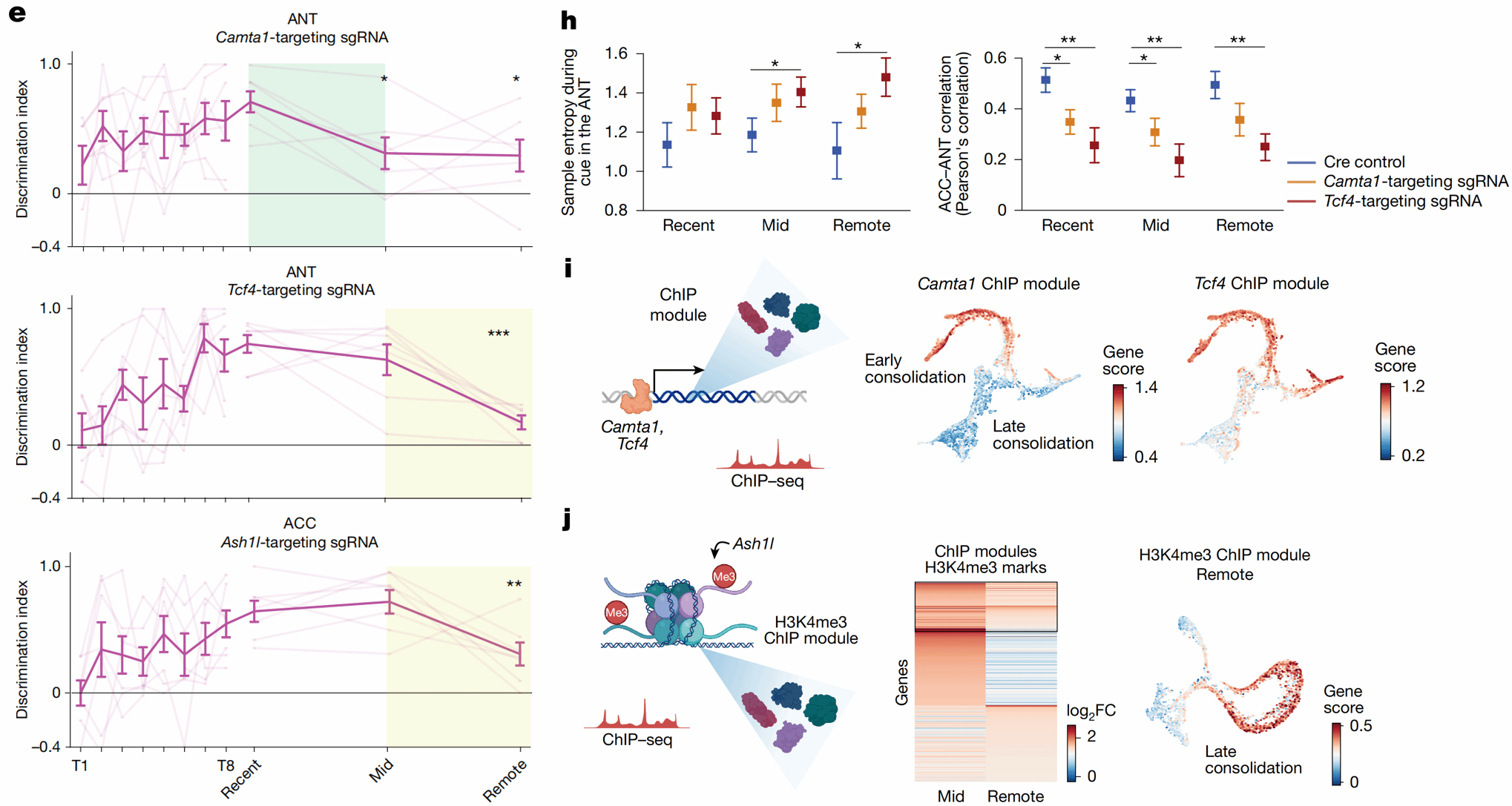
图4 Camta1-Tcf4-Ash1l丘脑–皮层转录级联对记忆稳定至关重要
总结
本研究建立了一种能够区分“深刻记忆”和“短暂记忆”的行为范式,并揭示了跨丘脑–皮层的Camta1-Tcf4-Ash1l转录级联在长期记忆巩固中的核心作用。研究发现,记忆巩固并非单一脑区完成的,而是一个跨脑区的“接力”过程:HPC中Creb1依赖的早期分子级联启动近期记忆形成;ANT中的Camta1和Tcf4将记忆延长至数天;ACC中的Ash1l则在更长时间尺度上稳定皮层神经元的记忆表征,驱动记忆的长期保存(图5)。这一跨脑区分子–环路网络揭示了记忆如何得以长期保存,同时为认知障碍相关疾病的潜在干预提供了新的方向。
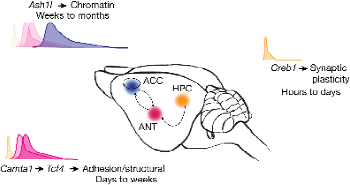
图5 Camta1-Tcf4-Ash1l转录级联在记忆稳定中的调控模型
原文链接:https://www.nature.com/articles/s41586-025-09774-6
参考文献
[1] Igaz, L. M., Vianna, M. R. M., Medina, J. H. & Izquierdo, I. Two time periods of hippocampal mRNA synthesis are required for memory consolidation of fear-motivated learning. J. Neurosci. 22, 6781–6789.
[2] Lamprecht, R. & LeDoux, J. Structural plasticity and memory. Nat. Rev. Neurosci. 5, 45–54 (2004).
[3] Nader, K. Memory traces unbound. Trends Neurosci. 26, 65–72 (2003).
作者:李伟广组 林圣洁