你是否发现,随着年龄增长,有些人会出现记忆力下降、反应变慢等问题?这背后,大脑白质的退化可能是关键推手1。这种变性包括轴突变性、脱髓鞘、小胶质增多和星形胶质病,这些都会损害神经传导,并产生不利于白质维持的炎症环境 2;更值得关注的是,负责生成和修复髓鞘的少突胶质细胞对缺血缺氧极为敏感,而髓鞘的维护与修复本身就是一项高耗能过程,一旦能量供应不足,白质损伤便会加速发生3。因此,血流对白质功能的维护非常重要。白质就像大脑内部的 “高速公路网”,由无数包裹着髓鞘的神经纤维组成,负责传递不同脑区之间的信号。而支撑这套 “高速网” 运转的,是一套精密的微血管系统 —— 其中,一种名为 “皮质主静脉”(PCV)的特殊血管,扮演着 “排水总管” 的角色,专门负责排出大脑深层组织的血液。
过去,科学家们一直争论:是血管供血减少导致了白质退化,还是白质退化反过来影响了血管功能?2025年8月12日西雅图儿童医院研究所、伯尔尼大学 ARTORG 生物医学工程研究中心、艾伦脑科学研究所、宾夕法尼亚州立大学等机构联合在《Nature Neuroscience》发表名为“Impaired capillary–venous drainage contributes to gliosis and demyelination in mouse white matter during aging ”上的研究给出了明确答案:血管排水系统的 “堵车”,是驱动白质衰老的重要原因。随着年龄增长,PCV 分支下的毛细血管会逐渐收缩、减少,导致大脑深层组织供血不足,进而引发炎症、髓鞘损伤等一系列问题,最终影响认知功能。
简单来说,大脑深层的毛细血管就像 “小巷”,PCV 是 “主干道”。年轻时 “小巷” 通畅、“主干道” 高效,血液能快速排出;年老后 “小巷” 变窄、甚至消失,血液淤积在深层组织,“高速网”(白质)因缺乏充足养分和氧气而逐渐 “老化失修”。更关键的是,研究通过实验证实,只要人为制造类似的轻微供血不足,就能在年轻小鼠身上重现衰老相关的白质损伤,这为干预衰老提供了新靶点。
从血管结构到衰老机制的完整揭秘
(一)研究背景:白质衰老的 “鸡生蛋” 难题
大脑白质退化是衰老相关认知下降的核心特征之一,表现为髓鞘脱落、神经胶质细胞活化(炎症反应)、轴突损伤等。由于少突胶质细胞对缺血高度敏感,且髓鞘修复过程耗能巨大,年龄增长带来的脑血流量减少与血管稀疏现象,常被认为与白质退化相关。但长期以来,学界始终存在一个关键争议:脑血流量减少究竟是导致白质退化的诱因,还是白质退化引发的结果?
由于人类研究难以直接观察微血管的动态变化,且无法建立因果关系,研究团队选择用小鼠作为模型,结合深穿透多光子成像、光片成像、计算机模拟等技术,从微观血管结构入手,全程追踪衰老过程中大脑深层血管的变化,以及这些变化如何影响白质功能。
(二)核心发现 1:大脑里的 “专属排水总管”——PCV 的特殊结构
大脑正常供血循环是维系脑功能稳态的核心闭环:富含氧气与营养的血液经颈动脉、椎动脉进入颅内后,逐级分支为穿透性小动脉,像细密的 “养分输送管网” 深入大脑各皮质层及白质区域,在毛细血管网处完成与脑组织的养分传递及代谢废物交换;随后,表层组织的血液汇入普通静脉,深层组织的血液则通过专属引流通道集中回流,最终所有静脉血汇流后经颈静脉返回心脏,形成持续高效的 “供血 - 交换 - 回流” 循环,为神经元、髓鞘等关键脑结构提供稳定且充足的代谢支持。
为破解 “年龄增长过程中,大脑白质减少与脑血流下降究竟孰因孰果” 这一长期争议,本研究借助小鼠深部多光子成像技术,对皮质第 6 层及胼胝体中髓鞘化组织的微血管网络展开了精准解析。研究首次明确识别出一类稀疏却分布广泛的特殊静脉 —— 皮质主静脉(PCV),它们作为深层组织专属的 “血液引流中枢”,专门负责导出大脑深层区域的血液,而且其结构与人类大脑皮质和 U 形纤维(表层白质)交界处的血管系统高度相似,为跨物种机制研究提供了关键支撑。
进一步研究证实,PCV 是连接大脑深层组织与表层血管的核心 “枢纽”,其独特性体现在:
·结构特征 :PCV 呈圆锥形,主干贯穿所有皮质层,深层分支延伸至白质( corpus callosum,胼胝体,大脑最大的白质束),并随着组织深度的增加而延伸出越来越长的分支(图1a-b),且仅占所有上升静脉的 3%-4%,却承担了深层皮质和白质的主要血液引流任务(图 1g-i )。
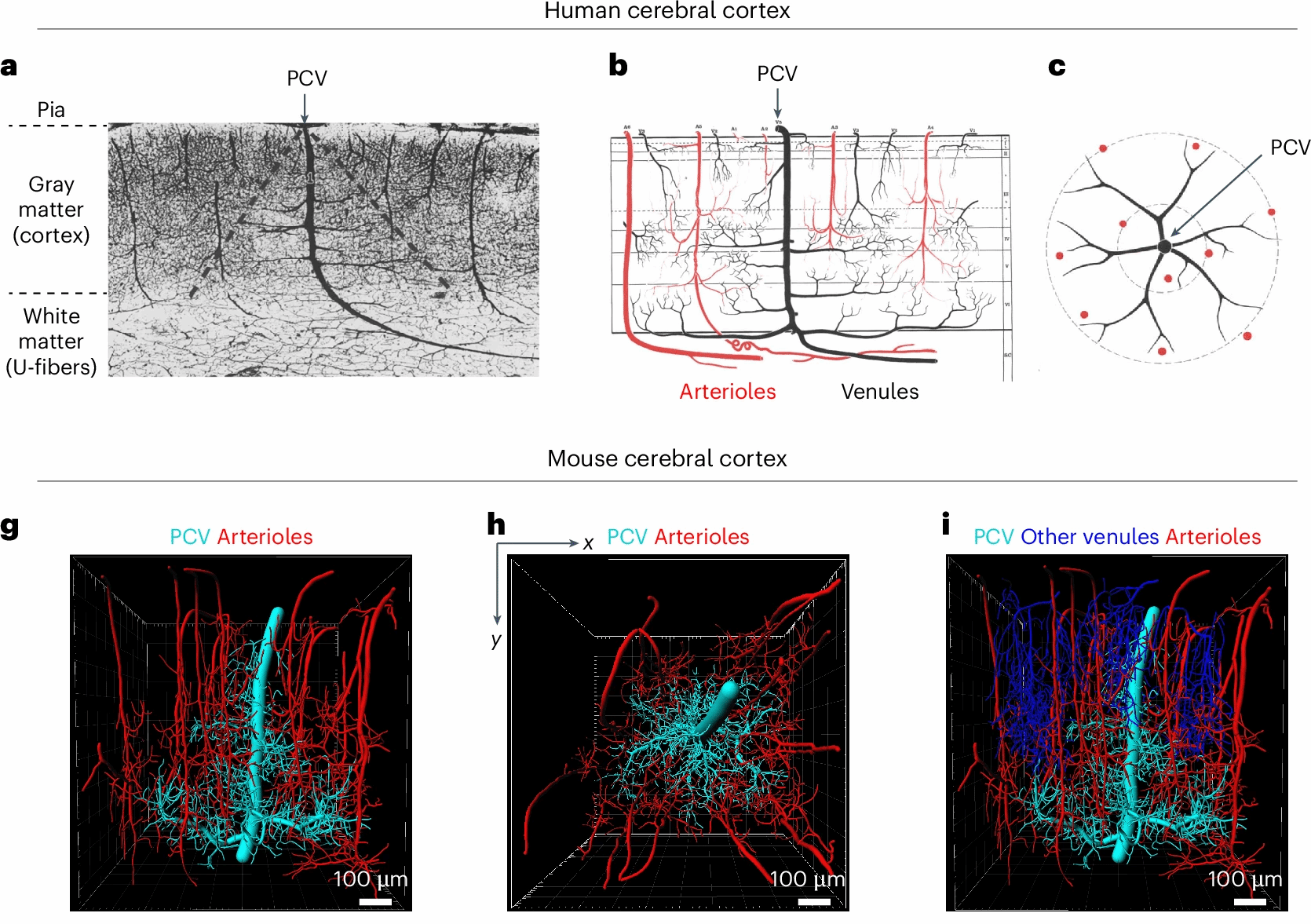
图1 人类和小鼠皮层中的 PCV
·分布规律:PCV 稀疏但位置关键,多分布在大脑主要感觉皮层区域(如躯体感觉皮层、视觉皮层),每个功能区通常只有一个 PCV,像 “专属排水总管” 一样服务于特定脑区(图 2j-l )。
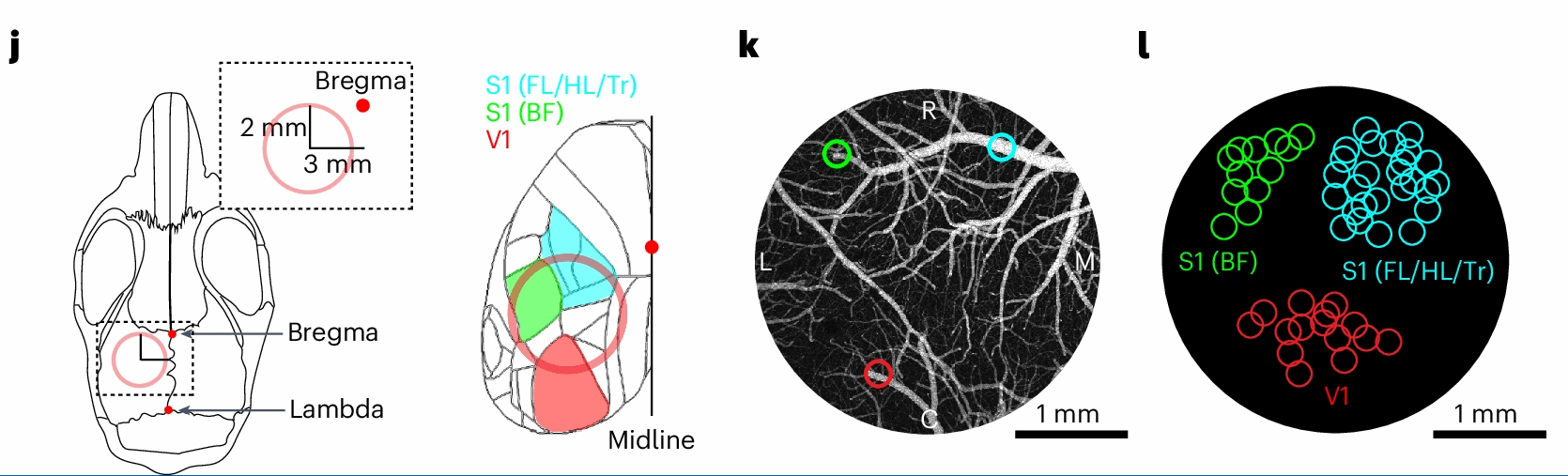
图2 人类和小鼠皮层中的 PCV
·人鼠共性:小鼠的 PCV 结构与人类大脑皮层和 U 型纤维(表层白质)交界处的血管高度相似,意味着研究结果对人类具有重要参考价值。
(三)核心发现 2:衰老导致深层毛细血管 “收缩 + 消失”,引发供血不足
通过深层活体双光子成像技术对比成年小鼠(5-7 个月)和老年小鼠(22-24 个月)的血管结构,研究发现了PCV 结构的年龄相关特异性变化:
·毛细血管减少:深层组织的血管长度密度下降,血管分支复杂度降低(如从 9 支血管组成的分支简化为 3 支),部分毛细血管因血流停滞而逐渐退化消失(图 3d,e)。
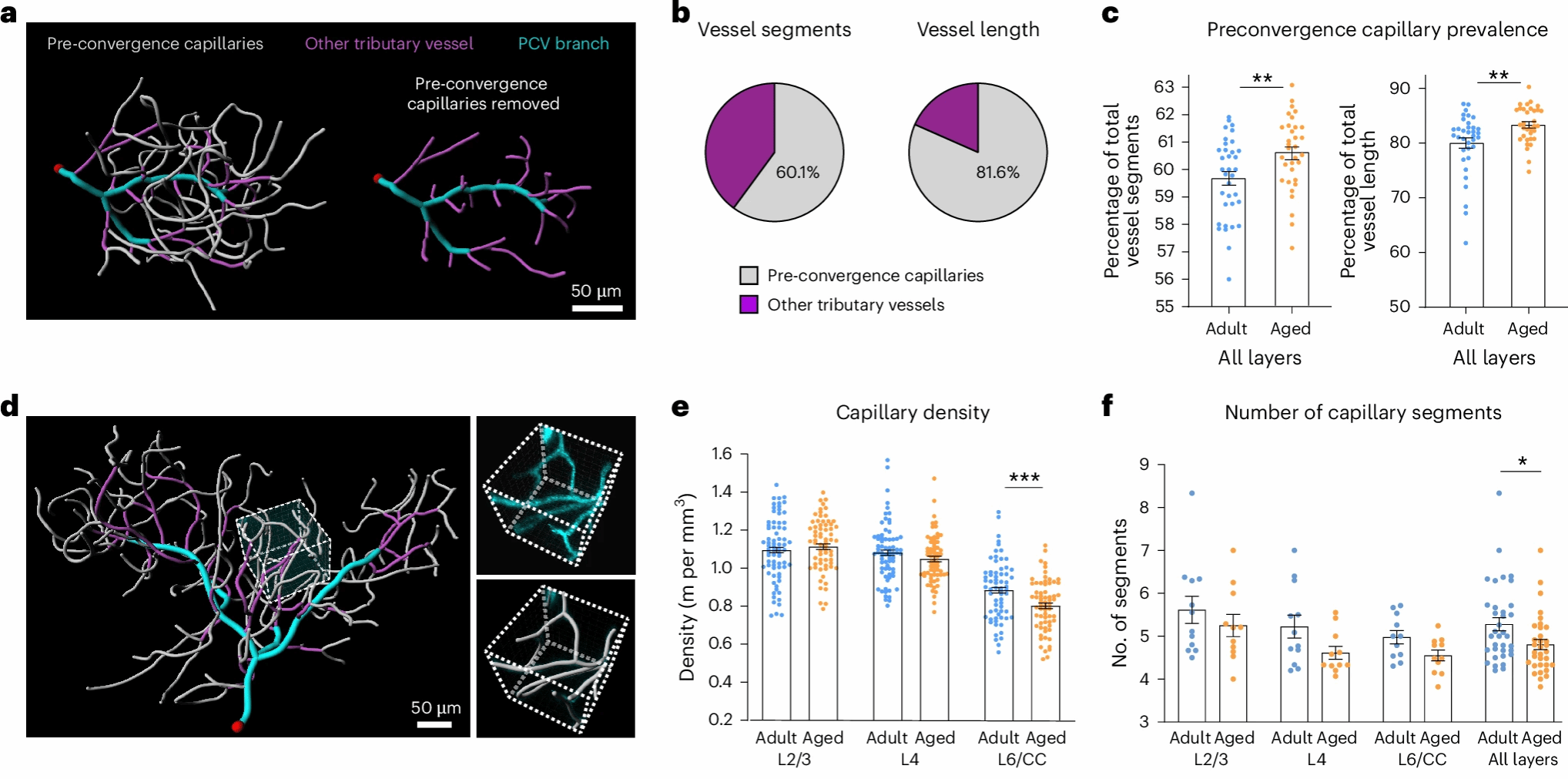
图3 老年小鼠血管密度降低,PCV 分支结构简化
·血流 redistribution:血液从深层组织 “转移” 到表层皮质,导致深层白质出现轻度但持续的供血不足(红细胞通量减少约 20%),而表层血流反而增加(图 4e、f)。
·毛细血管收缩:PCV 深层分支(对应皮质 6 层和胼胝体区域)的 “预聚合毛细血管”(连接动脉和静脉的关键血管)直径显著缩小,尤其是清醒状态下,老年小鼠该区域血管收缩更明显,而表层皮质血管反而轻微扩张(图 4d)。
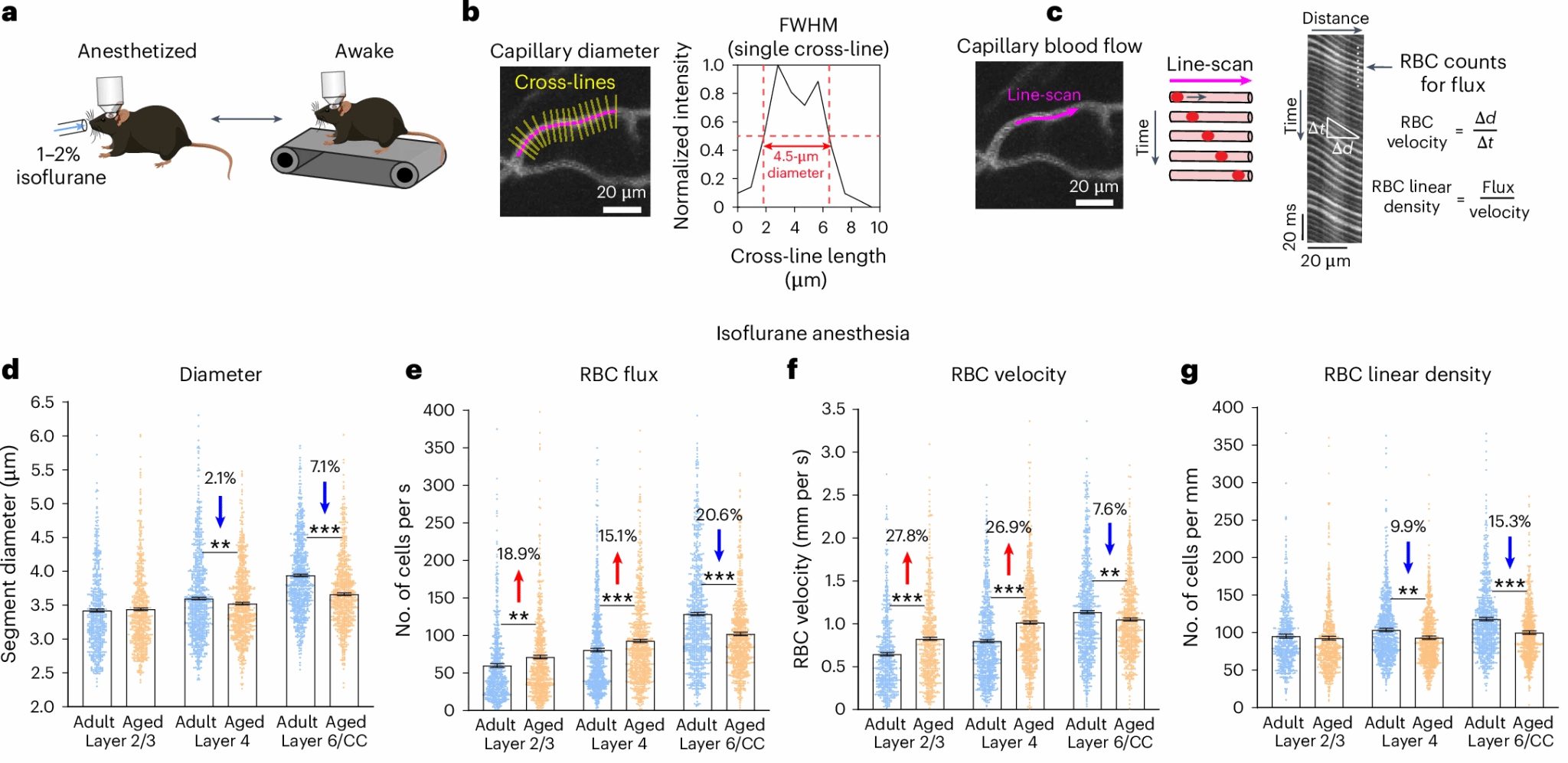
图4 衰老会引发第 6 皮质层 / 胼胝体区域特异性的血管收缩与血流不足
(四)核心发现 3:供血不足直接引发白质损伤,因果关系明确
随着年龄增长,汇聚前毛细血管会逐渐退化;为了验证 “供血不足导致白质衰老”,研究团队设计了两组关键实验:
1.毛细血管消融实验:用激光精准破坏成年小鼠深层的预聚合毛细血管(图5a、b),发现不仅被破坏的血管会退化,其周围的毛细血管也会出现收缩和血流下降,且深层组织的损伤比表层更严重(血流减少 70% vs 50%)(图5e、g、h)。
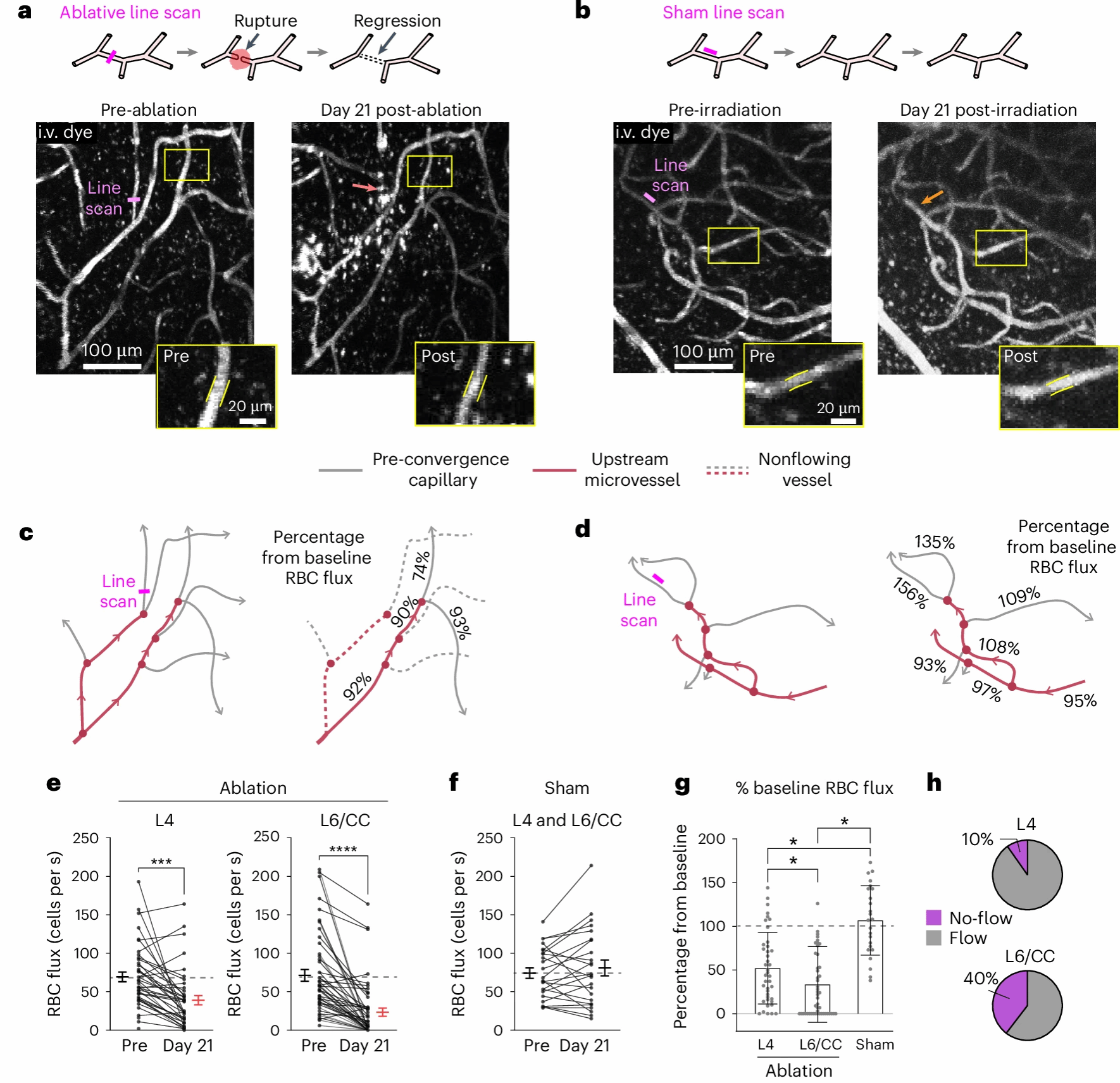
图5 在体损毁汇合前毛细血管可引发广泛血管收缩与低灌注
2.人为诱导供血不足:给成年小鼠实施单侧颈动脉狭窄手术(图 5a、b ),模拟老年小鼠的轻度供血不足(血流减少约 20%)(图 6c,d )。结果显示,21 天后,小鼠大脑深层白质出现明显的小胶质细胞活化(炎症)、星形胶质细胞增生(图 6e,f,i,j ),髓鞘完整性也受到破坏(图 6g,k ),与老年小鼠的病理变化完全一致。
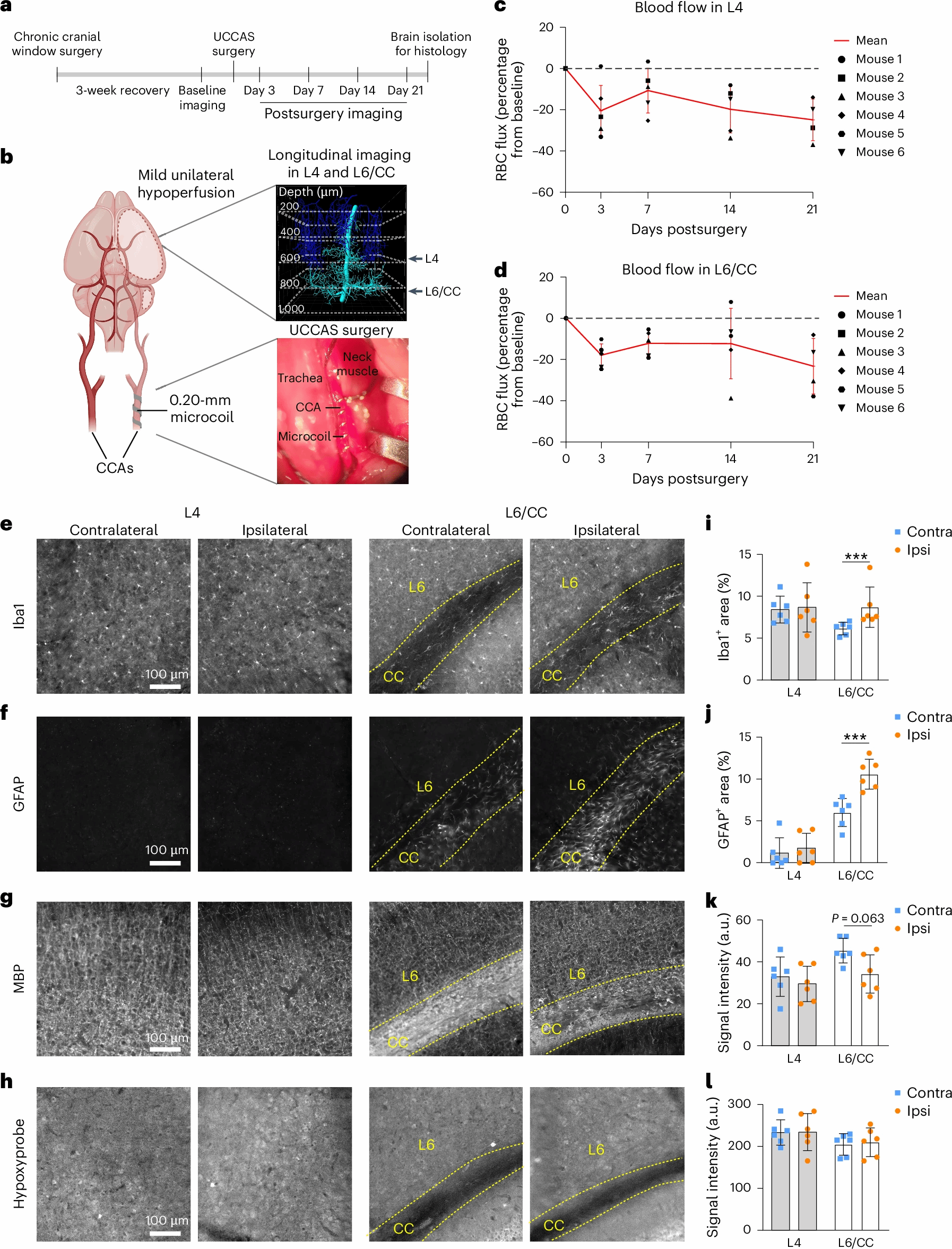
图6 在体损毁汇合前毛细血管可引发广泛血管收缩与低灌注
这两组实验直接证明:轻度供血不足是白质衰老的直接原因,而非结果。
(五)核心发现 4:低灌注引发的组织病理变化:白质的 “连锁损伤”
研究通过免疫染色等技术,明确了低灌注与组织病理的直接关联,主要表现为三大核心损伤:
1.神经胶质细胞活化(炎症反应)与髓鞘脱失:低灌注会过度激活本应参与组织修复的小胶质细胞(Iba1 标记)和星形胶质细胞(GFAP 标记),引发慢性炎症并破坏脑组织微环境,同时导致对氧和营养需求极高的髓鞘合成、修复受阻,表现为髓鞘碱性蛋白(MBP)信号强度下降,神经纤维失去 “绝缘保护”。老年小鼠深层白质中 Iba1 + 和 GFAP + 区域面积显著增加,且与低灌注程度高度相关,MBP 信号强度则明显降低(图 6a-c);人为诱导轻度低灌注后,成年小鼠也会出现类似的炎症激活和髓鞘损伤。
2.血管内皮炎症:低灌注还会引发血管内皮损伤,老年小鼠白质中血管细胞黏附分子 1(VCAM1)表达显著升高,这种分子会促进白细胞黏附在血管壁上,进一步加重血管堵塞,形成 “低灌注→内皮损伤→更严重低灌注” 的恶性循环(图 7d-g)。
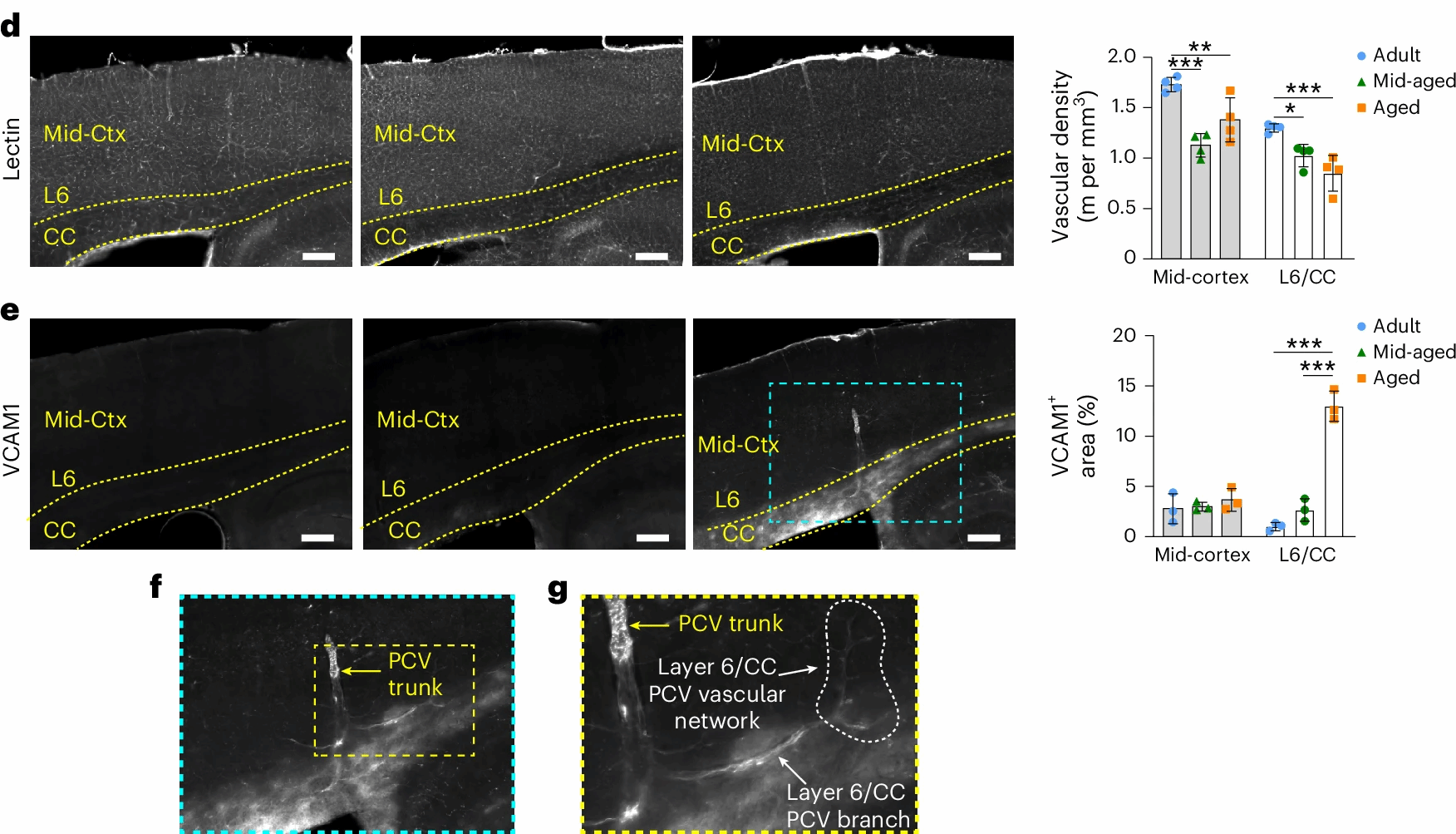
图7 轻度单侧低灌注足以诱导同侧胼胝体发生神经胶质增生与髓鞘脱失
值得注意的是,这种损伤并非源于严重缺氧(实验未检测到明显缺氧信号),而是长期的 “代谢供给不足”—— 就像一辆汽车长期低速行驶,虽未熄火,但发动机逐渐磨损。
这项研究通过多技术融合(活体成像、手术干预、计算机模拟),清晰揭示了大脑衰老的一个关键机制:皮质主静脉(PCV)深层分支的毛细血管收缩、退化,导致白质供血不足,进而引发炎症和髓鞘损伤。
这项研究让我们认识到,大脑深层微血管的 "排水系统"——PCV 的功能异常,是连接血管衰老与认知衰退的关键纽带。从识别 PCV 的特殊功能,到明确其在衰老中的核心作用,再到通过实验验证因果关系,科学家们一步步揭开了大脑衰老的神秘面纱。这一发现不仅解答了长期以来的学术争议,更让我们意识到:保护认知功能,要从保护大脑血管做起。通过控制基础疾病、坚持适度运动、保持健康饮食和生活习惯,我们就能在日常生活中为大脑微血管 "减负",延缓其功能衰退,让大脑在老年依然保持活力。未来,随着对 PCV 机制的进一步探索,相信会有更多精准的诊断技术和治疗方案出现,让“健康老龄化”不再是奢望。
参考文献
[1] Gunning-Dixon, F. M., Brickman, A. M., Cheng, J. C. & Alexopoulos, G. S. Aging of cerebral white matter: a review of MRI findings. Int. J. Geriatr. Psychiatry 24, 109–117 (2009).
[2] Groh, J. & Simons, M. White matter aging and its impact on brain function. Neuron 113, 127–139 (2025).
[3] Dewar, D., Underhill, S. M. & Goldberg, M. P. Oligodendrocytes and ischemic brain injury. J. Cereb. Blood Flow. Metab. 23, 263–274 (2003).