背景
光,是一种古老的信号,而当它诞生在生物体内,则会成为一种有力的信号:夏夜的萤火虫交织漫游、海浪里的磷虾成群起舞、深海里的生物彼此试探……
而在动物的大脑深处,也存在着类似的微光。当神经元活动、信息流动,细胞内的钙离子悄然起伏——那是一种看不见的“闪光”,承载着感知、思考与行为的瞬间。如果这些微小的变化,能够像萤火虫一样自己发光,会发生什么?
如今,研究者正在尝试用生物发光这一来自自然的语言,让大脑在黑暗中亮起来。不需要外界照射,不依赖强光刺激,神经元在活动时自行发出微弱却清晰的信号。研究者们得以长时间、温和地注视清醒动物大脑中单个神经元的闪烁,仿佛在夜色中,静静观察一片属于思想的星空:这就是生物发光钙离子探针。
钙离子 (Ca⟡⁺) 是神经元和其它兴奋性细胞中最核心的第二信使之一。动作电位的发生、突触传递、基因转录调控——几乎所有快速而关键的细胞功能,都伴随着细胞内Ca⟡⁺浓度的瞬时变化。正因如此,如何准确、灵敏、长期地记录Ca⟡⁺动态,始终是神经科学和细胞生物学中的核心技术问题。
过去二十年,基于荧光蛋白的遗传编码钙指示器 (genetically encoded calcium indicator,GECI),极大推动了神经活动在体成像的发展[1],如GCaMP系列[2]和GECO家族[3],其中,GCaMP至今已迭代至第八代,至今仍是荧光蛋白类GECI性能的基准标杆。然而,荧光成像仍不可避免地依赖外部激发光,这带来了光毒性、自发荧光、组织散射以及在深部组织中信噪比下降等一系列问题[4]。这使得它们在长时间活体成像、深脑区域成像、或高度光敏实验体系中的应用并不理想。
而生物发光探针提供了一条不同的路径:它们无需外源激发光,背景噪声极低,理论上非常适合进行长期、低干扰的功能成像[5]。但现实是,现有的生物发光Ca⟡⁺探针普遍亮度不足、动态范围有限,难以捕捉快速而微弱的Ca⟡⁺变化,这使得它们始终未能真正成为主流的神经成像工具。
近日,发表于 Nature Methods 的一项研究中,研究者开发了一种全新的高对比度生物发光钙指示器——CaBLAM (Calcium Bioluminescence Activity Monitor)。该探针基于工程化的 Oplophorus gracilirostris 萤光素酶[6]变体构建,在亮度、动态范围和Ca⟡⁺响应速度上实现了显著突破,为“无激发光”的功能成像提供了一个可用的解决方案。

CaBLAM 的设计与原理
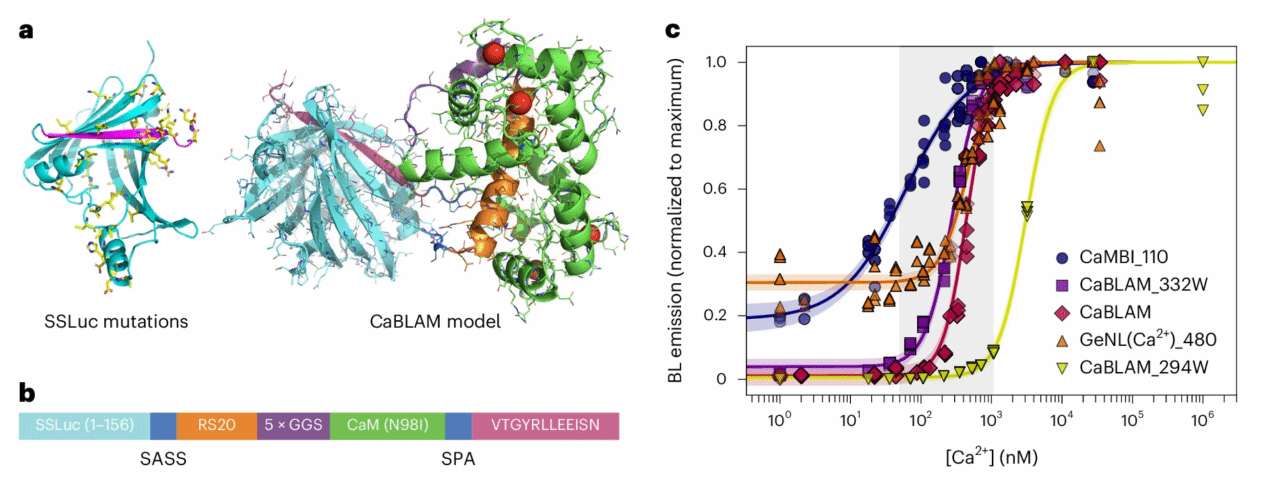
Fig. 1: CaBLAM architecture and Ca2+ affinity.
作者以OLuc突变体eKAZ[7]为起点,通过交替使用易错突变库和定点突变库在大肠杆菌中进行了多轮定向进化。每轮筛选均基于更高的蓝光发射强度和溶解度进行变体选择。后续作者还添加了如下工程改造:构建mNeonGreen[8]融合蛋白以提升发光量子产率;整合NanoLuc[9]和NanoBit[10]中发现的部分突变;优化C端肽序列;精细调节C端肽与蛋白质其余部分的相互作用。最终克隆体命名为SSLuc(图1a),而钙探针CaBLAM总体示意图如图1b,包括一个萤光素酶主体和一个钙感受模块(CaM-RS20),另有绿色荧光蛋白mNeonGreen作为 FRET 辅助。CaBLAM在体外表现出约83倍的信号对比度(+Ca⟡+vs -Ca⟡+),远超之前的生物发光 GECI(图1c)。
至此,CaBLAM的分子设计既实现了高对比度,又拥有合适的钙亲和性,为后续在细胞与体内使用打下了基础。
荧光共振能量转移 (fluorescence resonance energy transfer,FRET) 原理是指在供体和受体相互靠得很近(1-10 nm)时,光子能从一个供体转移到受体的过程。这种能的转移是非放射性的,其主要原因是供体和受体之间的偶极-偶极间的相互作用。因此,在萤光素酶的基础上,将多色荧光蛋白与之相连,可以利用FRET达到增强发光和改变发射光波长的效果。
CaBLAM 在细胞中的性能表现
随后,作者比较了 CaBLAM 和GCaMP8s在体外培养的细胞中的表现。
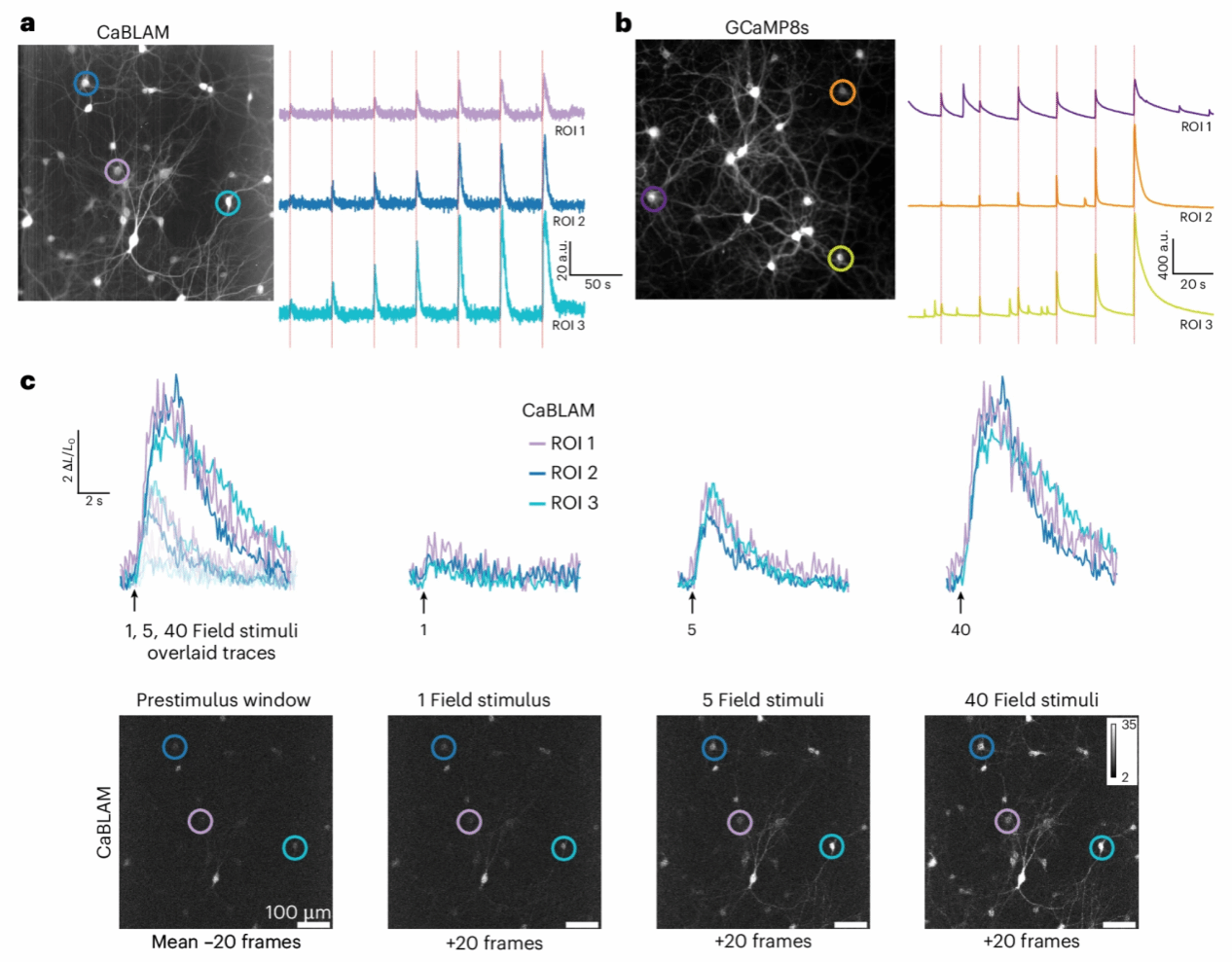
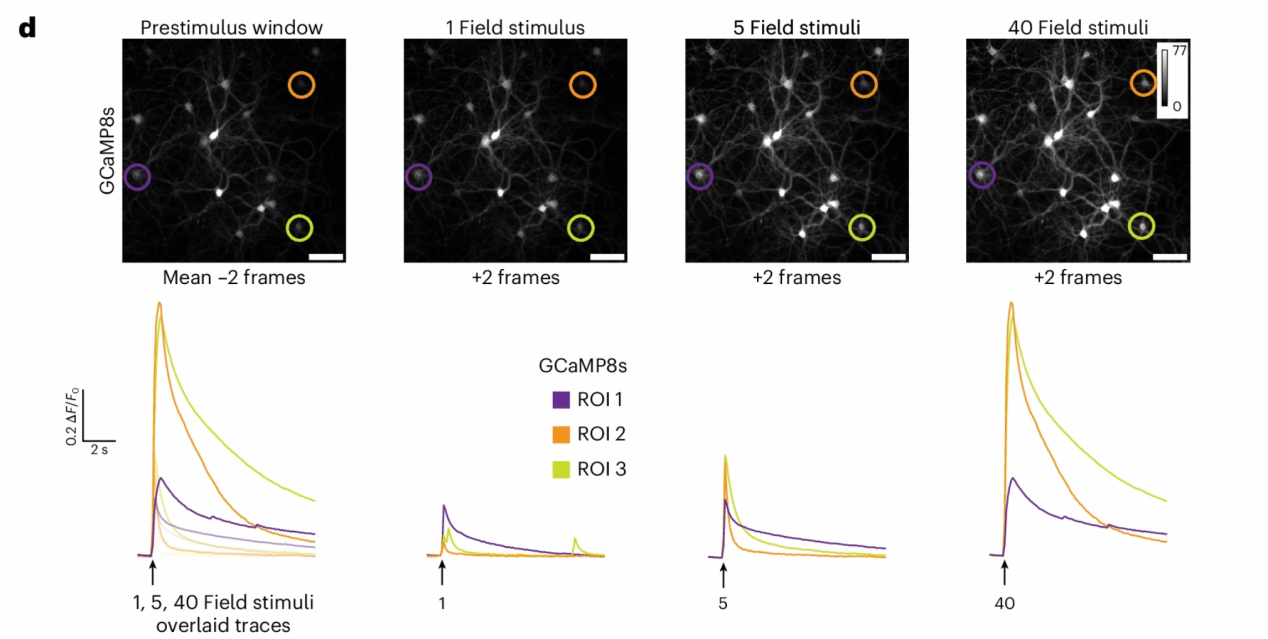
Fig. 2: Overview of a typical Ca2+ imaging session comparing electrical field evoked responses in CaBLAM- and GCaMP8-expressing rat hippocampal neurons.
在大鼠神经元中,表达CaBLAM的神经元比起GCaMP8s在10Hz成像期间显示出较低的可检测光子计数,但单个轨迹在电场刺激下同样呈现了可检测的诱发反应(图2a、b)。随后,作者又检测了表达CaBLAM和GCaMP8s的神经元细胞在刺激前、1次场刺激、5次场刺激及40次场刺激的条件下表现出的钙离子响应轨迹(图2c、d)。这些初步观察结果代表了两种指示剂典型响应特征,且由于GCaMP8s的基线信号较高,其荧光信号变化幅度(ΔF/F)显著低于CaBLAM的生物发光信号变化(ΔL/L)。
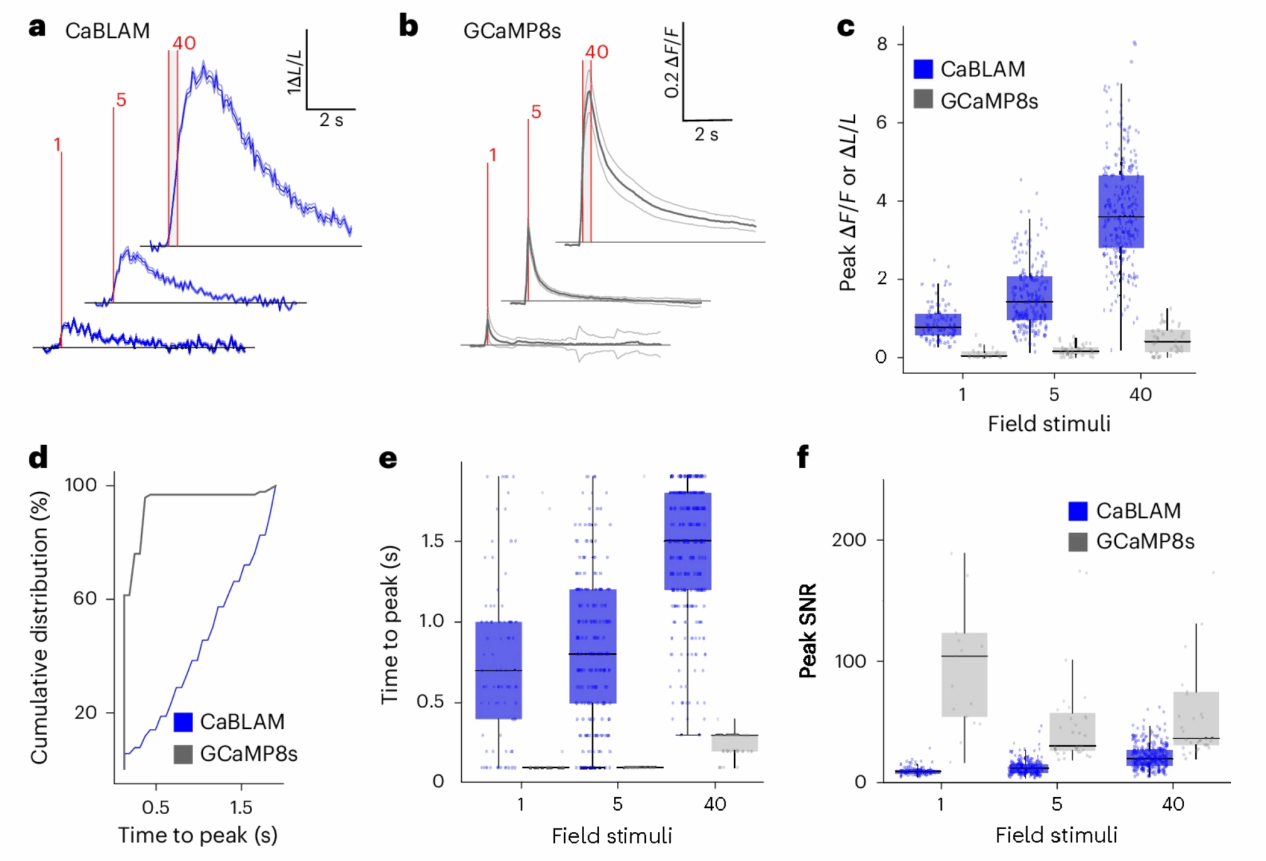
Fig. 3: CaBLAM provides high-contrast reporting of stimulus-evoked neural activity in cultured neurons.
作者随后对表达CaBLAM(图3a)和GCaMP8s(图3b)的神经元中刺激诱发的生物发光和荧光信号进行了表征。与初步观察一致,电场刺激(1、5和40次脉冲,频率约83Hz,脉冲宽度1ms)在CaBLAM中诱发的ΔL/L变化幅度显著高于GCaMP8s的ΔF/F变化,这得益于CaBLAM的基线信号较低(图3c)。此外,作者还测量了两种探针达到峰值ΔL/L(CaBLAM)和ΔF/F(GCaMP8s)所需的时间,并观察到明显的响应时间差异(图3d、e)。图3f则比较了CaBLAM与GCaMP8s的峰值信噪比(SNR)。尽管GCaMP8s的对比度低于CaBLAM,但在该场景下仍展现出更高的峰值信噪比,但当所检测的刺激较强时,它们的SNR差异相差不大。
经上述测试,作者证明了CaBLAM虽然在总体亮度上不占优势,响应动力学显著慢于GCaMP8s,但信号变化幅度比起GCaMP8s更为明显。总体来说,CaBLAM对神经元内生理范围的Ca⟡+变化足够敏感,响应速度足以反映神经活动节律,已经是一款能够在活细胞中作为钙信号读出工具工作的生物发光钙探针。
在活鼠大脑中监测神经活动
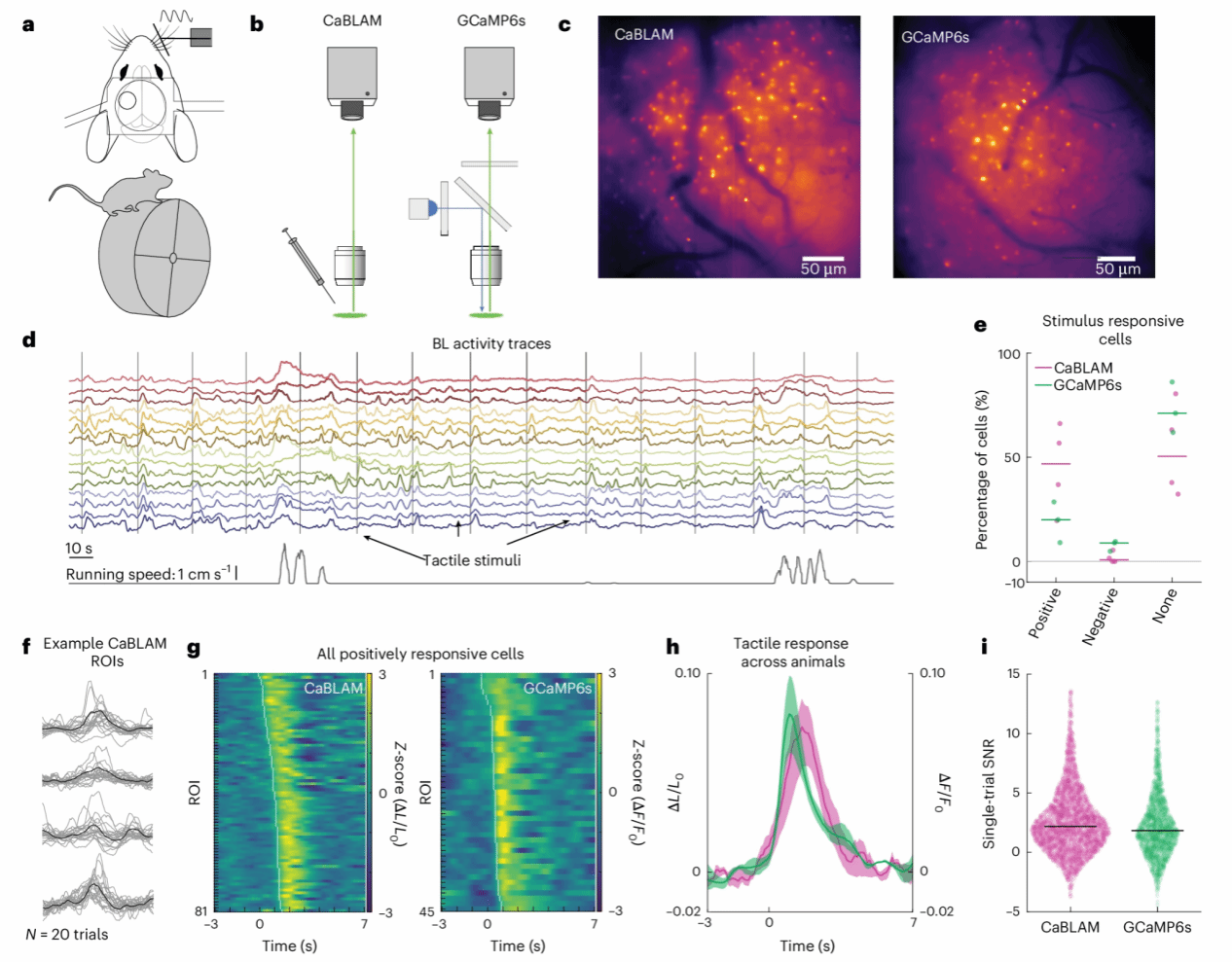
为了验证 CaBLAM 在真实神经系统中的表现,研究者将实验推进到了清醒、头固定、可自由奔跑的小鼠模型中。这里作者通过对神经元源性神经营养因子(NDNF)-Cre小鼠品系中标记的新皮质中间神经元(图4),对CaBLAM与GCaMP6s在体内的性能进行了表征与比较。经病毒选择性表达与手术准备后,分别在无外部光源(CaBLAM)及单光子荧光照明(GCaMP6s)条件下进行成像。所有小鼠均采用头部固定方式,允许自主奔跑,同时在体感皮层上方建立颅窗进行成像(图4a)。研究者对胡须区施加重复的触觉刺激,并同步记录神经元活动与小鼠的运动状态。这一范式确保所记录的信号来源于感觉诱发的神经活动,而非单纯的运动或状态变化。
CaBLAM 的成像在完全黑暗条件下进行;而作为对照,表达于相同神经元群体中的 GCaMP6s 则采用常规表照荧光方式成像(图4b)。两种传感器在相似视野和刺激条件下进行比较,使得信号特性可以直接对照。
从单个视野的成像结果可以看到,CaBLAM 在体感皮层浅层中清晰标记出大量 NDNF 神经元,并在触觉刺激到来时呈现出与刺激严格时间锁定的信号变化(图4c、d)。即便在小鼠奔跑、整体神经活动背景发生波动的情况下,这些刺激相关响应依然稳定存在。
对单细胞时间序列的分析显示,多次触觉刺激会在部分 NDNF 神经元中诱发高度一致的Ca2+响应。将多个细胞的信号按刺激时序叠加后,可以观察到一个清晰的群体响应模式,提示这些神经元在感觉输入过程中具有可靠而一致的激活特征。与近期研究结果一致[11],部分NDNF细胞对触觉刺激呈现正向(图4e、g–i)或负向反应,其反应强度受唤醒状态调节(图4j)。两个传感器组中响应最活跃的细胞大多受到触觉刺激的正向调节(图4f),其中CaBLAM组占比97%,GCaMP6s组占比72%。图4i显示,触觉诱发的两组探针在幅度和整体时域动态特征上高度可比,而图4h显示,CaBLAM响应起始延迟晚于GCaMP6s,与体外数据一致。
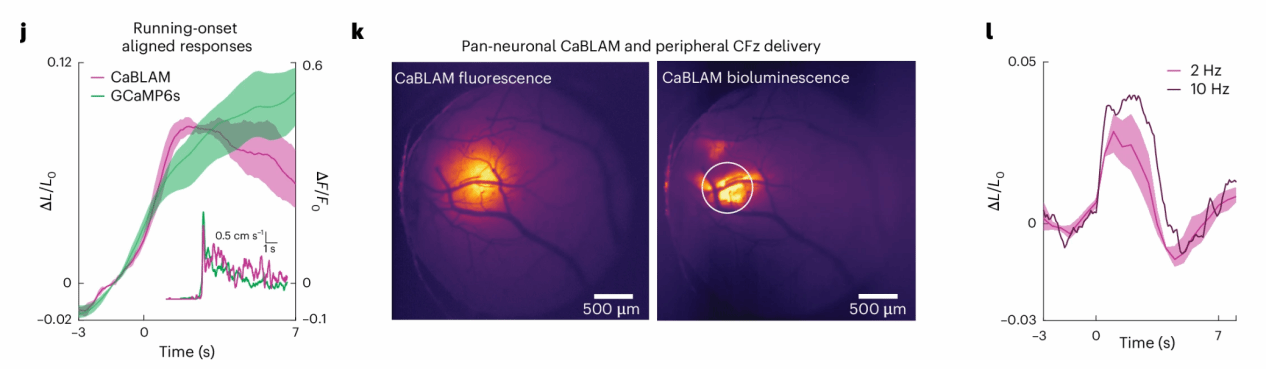
Fig. 4: CaBLAM shows SNR comparable to GCaMP under epifluorescent illumination during in vivo mammalian imaging.
在证明CaBLAM能够在体感皮层的NDNF神经元中可靠记录触觉诱发活动之后,作者进一步提出了一个对实际神经科学实验尤为重要的问题:在不进行局部颅内给药的情况下,CaBLAM是否仍然能够报告感觉驱动的神经动力学?为此,研究者采用了更接近常规实验范式的设计——外周给药。他们在全神经元水平表达CaBLAM(hSyn-AAV2/9),并通过眶后注射的方式向小鼠体内注射生物发光底物CFz(图4k)。随后,在清醒、头固定的小鼠中,对体感皮层进行大视野(约3.2 mm)生物发光成像。对群体平均信号的定量分析显示,所有小鼠的响应起始均发生在刺激开始后0.5秒以内。这一时间窗口显著早于常见的局部血流动力学变化(如血管扩张),说明CaBLAM记录到的信号主要反映的是神经活动本身,而非继发的血管或代谢效应。为了进一步刻画这种快速响应的时间结构,研究者将成像帧率从 2 Hz 提高至 10 Hz(图4l)。结果显示,在更高时间分辨率下,CaBLAM的响应在幅度和形态上与低帧率条件高度一致。
该实验说明,在无需颅内底物注射的情况下,CaBLAM依然能够以足够快的时间尺度,可靠地报告感觉驱动的皮层神经活动。
CaBLAM 在斑马鱼中的应用
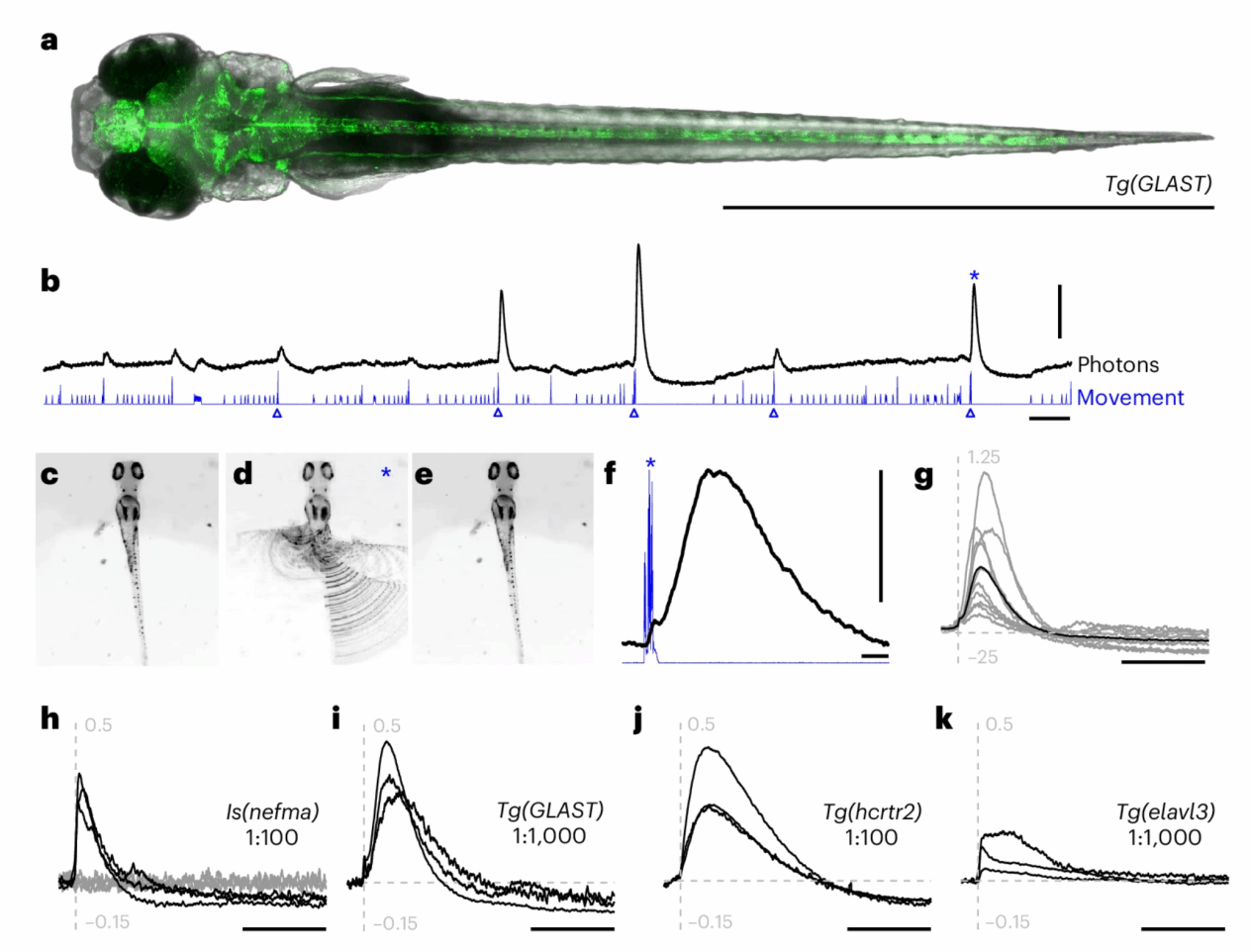
研究者构建了Tg(UAS:CaBLAM)斑马鱼转基因品系,并设计了一台简易显微镜,通过光子计数型PMT同步测量生物发光信号,同时利用机器视觉摄像头记录行为数据。CaBLAM在斑马鱼星形胶质细胞中表达(图5a),实验目的为测与自发性尾部运动相关的CaBLAM信号。微弱短暂的生物发光增强对应较小动作,而强烈持久的增强则伴随最大幅度动作(图5b)。大动作发生时段的视频帧(如图5c-e)显示,这些动作由强烈的非对称性、不协调尾部抽动构成。生物发光增强持续约10秒(图5f),振幅存在差异(图5g),且所有观测到的大幅度运动均伴随生物发光增强。数据表明,大振幅尾部运动可诱发源自CaBLAM的生物发光。其中,不同基因型在最大运动后均呈现相似的生物发光增强现象,但动力学特征各异(图5h-k),这提示CaBLAM能够在斑马鱼中区分不同细胞类型参与运动时的Ca2+动态模式。
Is(nefma):中脑/后脑下行运动前神经元与脊髓神经元
Tg(GLAST):星形胶质细胞
Tg(hcrtr2):部分神经元与脊索相关大泡细胞
Tg(elavl3):几乎所有成熟神经元
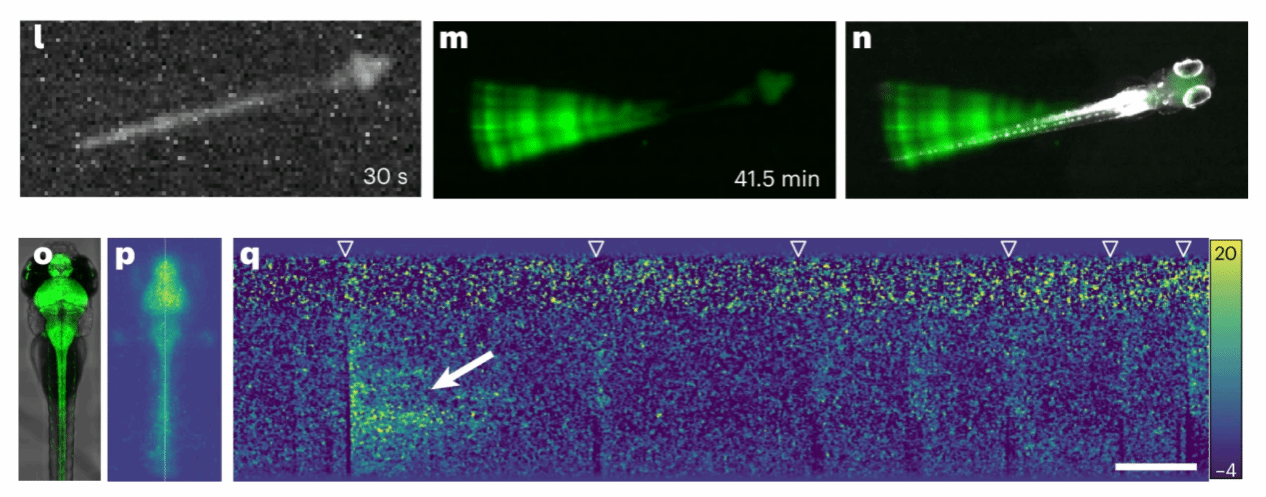
Fig. 5: CaBLAM-derived BL signals in astrocytes and neurons follow high-amplitude tail movements in head-embedded larval zebrafish.
此外,作者利用显微镜中的机器视觉相机,对受精后5天(dpf)的Tg(elavl3)转基因鱼进行成像。通过4×4像素合并技术进行30秒曝光,清晰呈现了脑部和脊髓的生物发光信号(图5l)。通过测量重复曝光(n=83次,耗时41.5分钟)中各像素的标准差,作者成功消除背景噪声,揭示了该实验中特定尾部基底方向的微小偏移(图5m)。叠加幼鱼红外照明图像(图5n)可显示鱼体与生物发光的对齐关系。因此得出结论:即使采用低成本、非制冷且未增强的相机,亦足以解析CaBLAM衍生的生物发光信号。
其次,作者采用增强型高速摄像机,测量头部固定的4 dpf Tg(elavl3)鱼的生物发光(图5o、p)。对鱼体中线进行2分钟成像所得的波形图足以分辨尾部运动时的每次游动(图5q)。在一次大幅度运动中,可以观察到尾部强度显著增强;并且尾部区域保持明亮的时间长于头部区域,这与钙离子波传播的特征相符。由此可见,CaBLAM可用于监测斑马鱼幼体神经元和星形胶质细胞中的钙离子流。同时,研究揭示了在头部固定的鱼类中,大振幅尾部运动后尾部区域会出现强烈且持久的钙离子流增加现象。
总结
本文设计了一个高对比、高亮度的生物发光Ca⟡⁺指示器 CaBLAM,其在细胞中呈现的变化与现有的GECI基准标杆GCaMP8吻合。CaBLAM技术具备在广泛应用场景中实现活动监测的独特优势。该技术能够在头部固定的小鼠模型中,持续数小时高分辨率记录多个独立神经元的信号,从而实现无需光损伤和漂白效应的可靠成像;并在清醒小鼠体内实现单神经元分辨率的Ca⟡⁺流成像,其信噪比优于单光子照射下的GCaMP6s。也就是说,我们可以连续好几个小时记录大量单个神经元的活动,而且不会因为照光而伤害组织、也不会出现信号变暗的问题。换句话说,它更温和,也更适合做长时间观察。
未来,如果能让CaBLAM发出的光再亮一些,就有望拍得更快、更深、更清楚;如果再开发不同颜色的版本,甚至可能在不做任何侵入操作的情况下,同时观察多个脑区,甚至不同器官,在行为过程中的活动变化。
参考文献
[1] Li J, Shang Z, Chen J H, et al. Engineering of NEMO as calcium indicators with large dynamics and high sensitivity [J]. Nat Methods, 2023, 20(6): 918-24.
[2] EROFEEV A I, VINOKUROV E K, VLASOVA O L, et al. GCaMP, a Family of Single-Fluorophore Genetically Encoded Calcium Indicators [J]. JOURNAL OF EVOLUTIONARY BIOCHEMISTRY AND PHYSIOLOGY, 2023, 59(4): 1195-1214.
[3] Zhao Y, Araki S, Wu J, et al. An expanded palette of genetically encoded Ca2+ indicators[J]. Science, 2011, 333(6051): 1888-1891.
[4] Suzuki K, Kimura T, Shinoda H, et al. Five colour variants of bright luminescent protein for real-time multicolour bioimaging [J]. Nat Commun, 2016, 7: 13718.
[5] BADR C E, TANNOUS B A. Bioluminescence imaging: progress and applications [J]. Trends Biotechnol, 2011, 29(12): 624-633.
[6] Inouye S, Watanabe K, Nakamura H, et al. Secretional luciferase of the luminous shrimp Oplophorus gracilirostris: cDNA cloning of a novel imidazopyrazinone luciferase[J]. FEBS letters, 2000, 481(1): 19-25.
[7] Inouye S, Sato J, Sahara-Miura Y, et al. Luminescence enhancement of the catalytic 19 kDa protein (KAZ) of Oplophorus luciferase by three amino acid substitutions[J]. Biochemical and Biophysical Research Communications, 2014, 445(1): 157-162.
[8] Shaner N C, Lambert G G, Chammas A, et al. A bright monomeric green fluorescent protein derived from Branchiostoma lanceolatum[J]. Nature methods, 2013, 10(5): 407-409.
[9] Hall M P, Unch J, Binkowski B F, et al. Engineered luciferase reporter from a deep sea shrimp utilizing a novel imidazopyrazinone substrate[J]. ACS chemical biology, 2012, 7(11): 1848-1857.
[10] Dixon A S, Schwinn M K, Hall M P, et al. NanoLuc complementation reporter optimized for accurate measurement of protein interactions in cells[J]. ACS chemical biology, 2016, 11(2): 400-408.
[11] Markopoulos F, Chéreau R, Brandalise F, et al. Neurogliaform cells mediate interhemispheric modulation of sensory-evoked activity in cortical pyramidal neurons[J]. bioRxiv, 2025: 2025.04. 30.651595.
作者:苏一驰组 史幸怡