一般而言,神经元的树突和胞体接收突触输入,在经过整合并达到一定的电压阈值后,在轴突始段(Axon initial segment,AIS)最先产生神经元的输出信号——动作电位(Action potential),主要是因为此处表达有非常高密度的电压门控Na⁺通道,其中相对低阈值的Na⁺通道亚型决定动作电位的爆发(Hu et al., Nat Neurosci 2009)。轴突一般不接收突触输入,但在特定种类的神经元上AIS也接收GABA能突触输入,这些突触能够调控动作电位的发放,参与觉醒状态的调节,并在癫痫、孤独症和精神分裂症等病理状态中发生改变。AIS是否也接收兴奋性的谷氨酸能突触输入呢?此前,人们在大鼠、猫、非人灵长类及人类等多个物种,以及皮层、海马等多个脑区神经元的AIS上观察到与树突棘(Dendritic spine)非常相似的突棘样结构,并将其命名为轴突棘(Axonic spine)。然而,轴突棘的超微突触结构、生理功能和环路作用都不清楚。
2026年5月15日,复旦大学脑科学转化研究院舒友生团队在《自然-神经科学》(Nature Neuroscience)期刊上在线发表题为《Excitatory synapses onto axonic spines jump-start action potentials and route information flow》的研究论文。该研究发现,在负责情绪调控与社交互动等行为功能的重要脑区——侧隔区(Lateral septum,LS)中,超半数的抑制性神经元发育有轴突棘结构,并从突触、细胞和神经环路多个层面解析了轴突棘的结构特征和功能作用。该论文将于六月以封面文章的形式正式出版。

研究团队首先利用全细胞膜片钳记录结合荧光染色,对LS神经元进行了电生理与形态学分析。结果发现,约60%的LS神经元在AIS存在突棘样结构。拥有轴突棘的神经元被称为Axonic-spine neuron(ASN),没有该结构的神经元则为non-ASN。进一步研究发现,在以GABA能神经元为主的脑区,如终纹床核(BNST)和纹状体(Striatum)中,同样约有60%的抑制性神经元存在轴突棘结构,提示该亚细胞结构可能广泛存在于中枢神经系统的抑制性神经元上。
在突触层面,研究团队通过扫描电镜对ASN进行了电镜超微结构重构,发现轴突棘的突触前结构中含有突触囊泡和活性带(Active zone),突触后膜存在明显的突触后致密区(Postsynaptic density,PSD),且PSD显著厚于活性带,具有典型的非对称突触特征。这些超微结构特征提示其为兴奋性谷氨酸能突触。结合双光子谷氨酸解笼锁(Glutamate uncaging)实验,发现在轴突棘上可诱发兴奋性突触后电位(EPSP),由AMPAR、KAR与NMDAR等离子型谷氨酸受体所介导。此外,通过脉冲时序依赖可塑性(Spike-timing dependent plasticity,STDP)的诱导实验,观察到轴突棘具有长时程结构可塑性,表现为轴突棘的颈部(Spine neck)缩短。
在细胞层面,研究团队利用Ankyrin-G抗体对AIS进行标记,并通过荧光及电镜成像证实轴突棘定位于AIS上。鉴于AIS是动作电位最容易产生的区域,相较于树突棘,轴突棘应该能够更快更有效地驱动动作电位的产生。单光子谷氨酸解笼锁实验显示,在较低强度刺激下,轴突棘诱发的EPSP明显强于树突棘;在中等强度输入时,轴突棘即可驱动动作电位产生,而树突棘尚不足以诱发放电;在高强度输入条件下,虽然两者均可触发动作电位,但轴突棘诱导的动作电位先于树突棘诱导的动作电位。这表明,相较于树突棘,轴突棘能在更低强度的谷氨酸输入条件下产生动作电位,且更快速地驱动神经元产生输出信号。进一步药理学结果提示,这一优势依赖于AIS上高密度电压门控Na⁺通道的激活。
在环路层面,研究团队利用mGRASP技术追踪轴突棘的上游来源,发现来自海马背侧CA3(dCA3)区域的投射可与LS神经元的Ankyrin-G信号共标,证明dCA3是LS轴突棘的重要上游脑区。同时,dCA3的投射也会到达LS神经元的胞体及树突。基于轴突棘具有更强、更快地驱动动作电位产生的能力,研究团队提出一种新的局部环路模型:来自dCA3的输入可优先激活ASN,使其率先产生动作电位,并通过前馈性抑制(feedforward inhibition)压制周围non-ASN神经元的电活动,从而实现信息在局部环路中的偏向性传递,即“路由器”功能。光遗传实验进一步证实,激活dCA3至LS的轴突投射后,发现侧隔区中ASN优先发放;而在加入GABA受体拮抗剂阻断抑制性突触传递后,发现ASN 的动作电位发放仍然显著早于non-ASN,提示其导致的快速侧抑制(Lateral inhibition)压制了周围的non-ASN电活动,从而仅ASN携带的信息可以被传递给下游脑区。
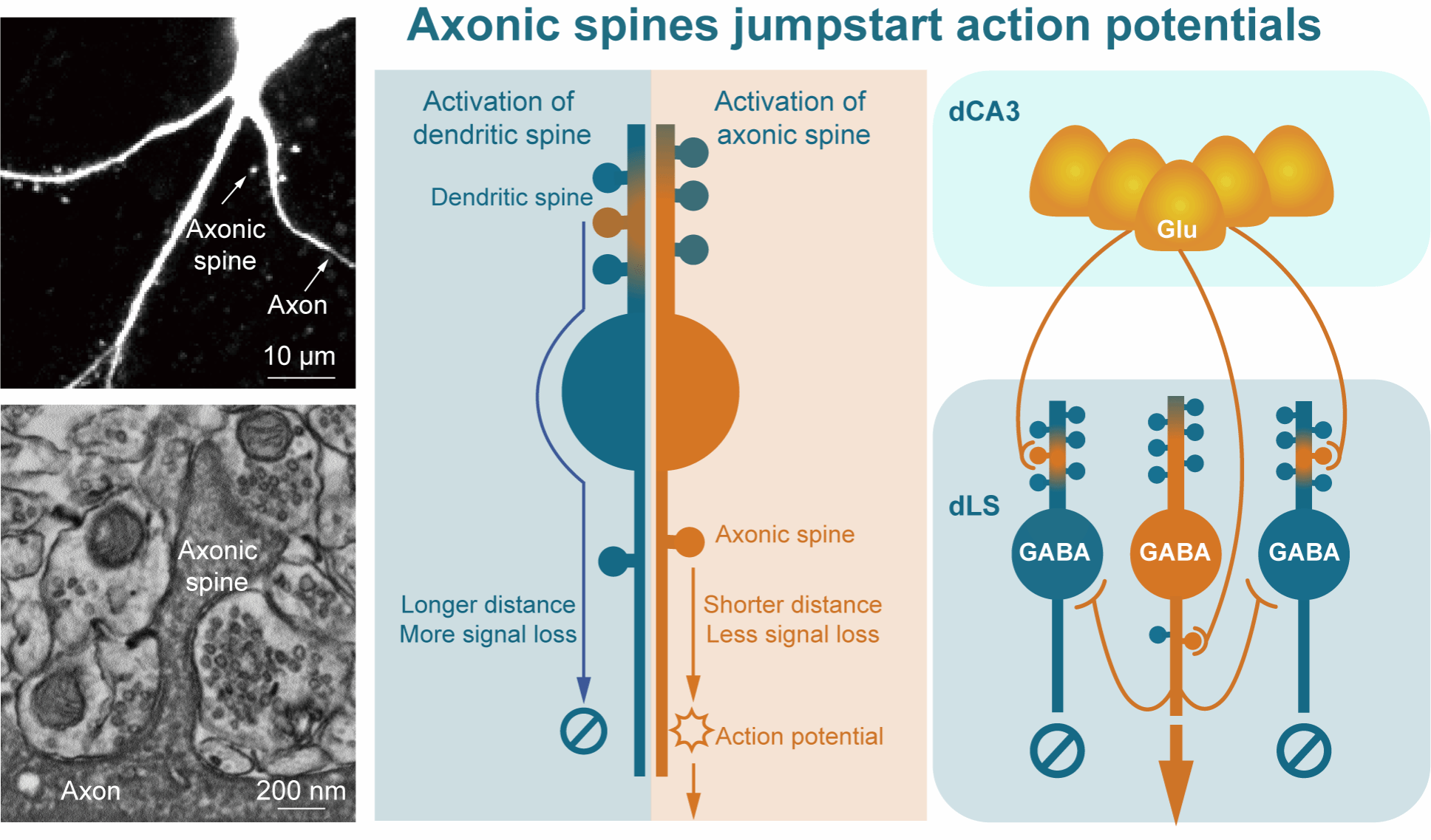
图1 轴突棘结构与功能示意图。左侧为轴突棘的双光子成像与电镜结构图。中间为轴突棘的细胞功能:相较于树突棘的EPSP要经过树突 和 胞体 ( 较长 的 传播 路径导致信号 严重衰减,参考 蓝色 箭头 ),轴突棘的EPSP可以直接激活轴突始段的 Na + 通道 并 产生动作电位, 因为 更短的 传播 路径确保信号 不易衰减 (黄色 箭头 )。右侧为轴突棘的环路功能:dCA3谷氨酸能轴突会投射到dLS 的 GABA能 神经元的轴突棘和树突棘,但会首先激活 轴突棘神经元( ASN ) ,进而迅速抑制周围的 非轴突棘神经元( non-ASN ) , 从 而实现环路中的信息分流作用。
综上,本研究发现LS中多数抑制性GABA能神经元具有轴突棘结构,首次验证了轴突棘能形成具有功能的兴奋性突触,并发现与树突棘相比,轴突棘可以更快更有效地驱动动作电位的产生,进而介导神经环路中的信息分流。上述研究拓展了神经生物学领域内对于轴突棘超微结构与生理功能的认识,为探究轴突始段的功能提供了不可或缺的新视角。轴突棘这一重要细胞结构及其生理功能的发现,也为人工智能芯片设计和神经计算提供类轴突棘信息处理新模式。
复旦大学脑科学转化研究院舒友生教授为本论文的通讯作者。课题组博士后杨洪坤为该论文的第一作者,课题组博士研究生王坤、柯蔚副研究员、李俍博士、王舒扬博士,南京大学生命科学学院陈熠杰等做出了重要贡献。复旦大学脑科学研究院邰一琳研究员、何苗研究员,北京大学基础医学院神经生物学系张勇研究员,复旦大学脑科学转化研究院谭超研究员、李博研究员、博士研究生张文馨,复旦大学附属华山医院神经内科王坚教授、郁金泰教授,中国科学院脑科学与智能技术卓越创新中心孔妤博士、王旭博士等对该工作给予了大力支持。本研究得到科技创新2030-重大项目、国家重点研发计划、国家自然科学基金以及上海市优秀学术带头人项目的支持。