【导语】
微风拂面、刷牙洗脸,对普通人是日常,但对三叉神经痛(Trigeminal Neuralgia, TN)患者却是如电击、火灼般的噩梦。长期以来,我们虽知其痛,却难寻其源。近日,我院邓娟/孙立婷团队在《Advanced Science》发表研究,通过对脑干环路的全面解析,精准锁定了驱动这一剧痛的关键分子—Tac1。

一、“天下第一痛”:难以言说的顽疾
尽管目前的药物治疗(如非选择性钠离子通道阻滞剂卡马西平及奥卡西平)能在一定程度上缓解TN症状,但仍有约三分之二的TN患者在长期治疗后会陷入中重度疼痛的困扰,表现为药物耐受或出现焦虑抑郁等心理障碍,且药物治疗还伴有眩晕、疲劳、肝功能损伤等副作用。
与火热的躯体感觉机制研究不同,长期以来人们对于头面部感觉信息处理系统的了解仍停留在较模糊的水平,即仅知道外周感觉通过三叉神经节(Trigeminal ganglion, TG)经脑干向中枢传递信息,对于如TN、偏头痛等头面部相关慢性疼痛疾病更鲜少有深入的研究报道。疼痛程度强烈如TN,其背后的神经机制究竟隐藏在何处?这些问题一直困扰着生物医学界。
TN患者往往在微小的触碰下就会触发剧痛,这种异常现象提示我们,大脑处理颌面部痛觉的“阀门”出了问题。因此,研究团队将目光聚焦于颌面部信息传入中枢的必经之路—脑干,致力于解析清楚TN发展过程中的脑干神经环路机制。
二、锁定“信号中转站”:从Sp5C到PBN的环路
为了破解这一难题,该团队利用三叉神经痛小鼠模型(Chronic constriction injury of the infraorbital nerve, CION),结合单细胞测序、光遗传学、化学遗传学等前沿技术,展开了深入研究。为了收集到更多小鼠面部自发性及反射性行为,团队自主设计了适合小鼠面部行为检测的头部固定器,将原有的小鼠面部表情打分系统进行升级,同时利用von-Frey细丝检测机械痛阈,红外辐照检测热痛阈。
基于邓娟团队过去在躯体感觉研究中的神经环路机制发现,以及前人对于颌面部疼痛的研究,此次该研究团队将目光锁定在脑干中的两个关键部位:
臂旁核(Parabrachial nucleus, PBN):大脑中处理痛觉和情绪反应的核心枢纽。
三叉神经核尾核(Spinal trigeminal nucleus caudal part, Sp5C):负责接收颌面部痛觉信号的初始中转站。
首先,团队发现PBN尤其是腹外侧Tac1阳性神经元的激活对于CION模型引发的小鼠颌面部疼痛具有必要性。通过顺、逆行病毒示踪,团队发现,Sp5C浅层神经元密集投射向同侧PBN,化学及光遗传抑制或激活该环路可有效缓解或诱发小鼠颌面部疼痛,提示Sp5C-PBN环路形成了一条高效的“颌面部痛觉高速公路”。
三、关键分子:Tac1基因的特殊使命
为了解析向PBN投射的Sp5C神经元的细胞机制,研究团队应用了高精度单细胞测序分析手段Smart-Seq。结果惊讶地发现Sp5C这些投射神经元中,Tac1基因表达量最多。环路示踪结果进一步证明,这类Tac1阳性神经元可投射至同侧PBN脑区,体外电生理实验结果同时表明其可与PBN中Tac1阳性神经元形成兴奋性单突触功能连接。
当研究者应用基因敲降技术CRISPR-Cas9降低这些神经元中的Tac1表达,或者使用化学遗传学手段抑制Sp5CTac1-PBN环路时,TN小鼠的痛觉过敏行为得到了显著缓解。光遗传学激活Sp5CTac1-PBN环路及化学遗传学激活TG-Sp5CTac1环路则诱发小鼠显著的颌面部痛样行为。
研究结论:团队最终揭示了一条TG-Sp5C Tac1-PBN Tac1的神经环路,它是驱动三叉神经痛发生及发展的关键机制。
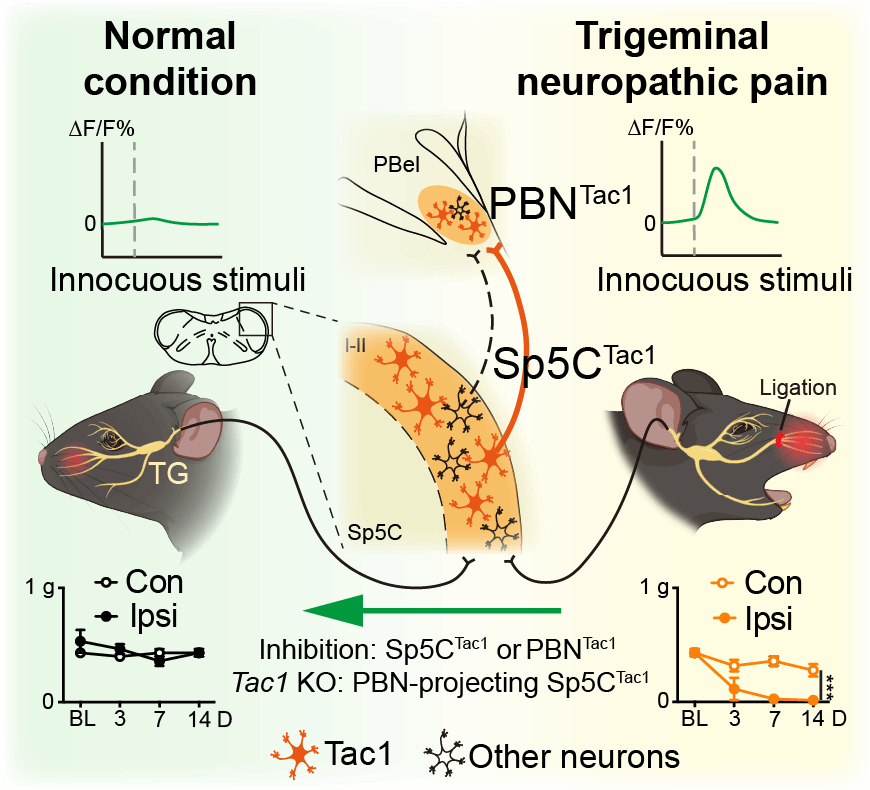
图1 三叉神经痛发展过程中,PBN的Tac1阳性神经元更易响应于非伤害性刺激;Sp5C中Tac1阳性神经元可将三叉神经节TG上行的颌面部信息传递至PBN。抑制Sp5C或PBN中的Tac1阳性神经元、抑制Sp5C-PBN环路、或敲低投射至PBN的Sp5C投射神经元中的Tac1基因,均可缓解CION模型引起的小鼠颌面部疼痛。
四、科学意义:解析颌面部痛觉机制的新视角
通过对脑干环路的系统梳理和对Tac1分子的深入挖掘,本研究不仅绘制出了一幅清晰的三叉神经痛上行传递地图,更从分子层面解析了痛觉过敏的本质。
这一成果不仅深化了我们对三叉神经痛发病机制的理解,也为未来寻找更具针对性的治疗手段提供了重要的科学依据。
【结语】
该研究成果以“A Tac1-Expressing Brainstem Pathway Underlies the Pathogenesis of Trigeminal Neuralgia”为题,于2026年3月13日在线发表于《Advanced Science》。
原文链接:https://doi.org/10.1002/advs.202516310。
复旦大学脑科学转化研究院青年副研究员孙立婷、博士生王佳佳、李翔宇为共同第一作者,课题组博士生林昕怡、李娟,本科生余秋瞳、王子涵对课题作出了重要贡献,课题同时得到了脑科学转化研究院程田林研究员和临港实验室金磊研究员团队的大力支持。邓娟青年研究员与孙立婷青年副研究员为本文的共同通讯作者。
本项目受到科技创新2030-重大项目(No. 2022ZD0207300)以及国家自然科学基金(Nos. 31825013, 82101320, 82222020)的资助。